���㣺��ѧƽ��ļ���,���ȷ�Ӧ�ͷ��ȷ�Ӧ,��Ӧ���ʵĶ�����ʾ����,��ѧƽ���Ӱ������
ר�⣺�����������������
��������1���ٸ������������ʵ��������û�ѧ������֮�ȵ������ʵ���֮�ȼ��������̼�����ʵ�������v=
����v��CO
2����
�����ڷ�Ӧǰ�������������䣬��650��ʱ��ʼ����4molCO��2molH
2O�뿪ʼ����2molCO��1molH
2O�ǵ�Чƽ�⣬��650��ʱ��ʼ����2molCO��1molH
2O����ƽ��ʱ���������ʵ���Ϊ0.8mol��ʵ��2��ЧΪ��ʵ��1�Ļ���������2molCO��1molH
2O����ƽ����������¶ȵ�900��ʱ��ʵ��2�����������ʵ���Ϊ0.4mol��С��0.8mol��˵�������¶�ƽ�����淴Ӧ�����ƶ���
��2���ٸ��ݸ�˹���ɼ���Ŀ���Ȼ�ѧ����ʽ�ķ�Ӧ�ȣ�
�ڢ�FeOΪ���壬������С��Ӱ��ƽ���ƶ���
��900��ʱƽ��ʱ��FeO��ת����Ϊ40%���ݴ˼���μӷ�Ӧ��FeO�����ʵ���������������ʽ����ƽ��ʱ�����ʵ����ʵ������ٸ���k=
���㣻
��1000��ʱ��Ӧ���ʱ�900��죬����ƽ������ʱ��̣���ͼ1��֪�������¶�FeO��ת���ʽ��ͣ�ƽ�����淴Ӧ�����ƶ����������¶�H
2O��g��ת���ʽ��ͣ����������Ӱ��ת���ʣ�������Խϸ����Ӧ����Խ�죬�ݴ˻���ͼ��
���
�⣺��1���١�ʵ��1��6min����ƽ��ʱ��������1.6mol�����ݷ���ʽ��֪�����ɶ�����̼�����ʵ���=1.6mol����v��CO
2��=
=0.13mol/��L��min����
�ʴ�Ϊ��0.13mol/��L��min����
�ڡ����ڷ�Ӧǰ�������������䣬��650��ʱ��ʼ����4molCO��2molH
2O�뿪ʼ����2molCO��1molH
2O�ǵ�Чƽ�⣬��650��ʱ��ʼ����2molCO��1molH
2O����ƽ��ʱ���������ʵ���Ϊ0.8mol��ʵ��2��ЧΪ��ʵ��1�Ļ���������2molCO��1molH
2O����ƽ����������¶ȵ�900��ʱ��ʵ��2�����������ʵ���Ϊ0.4mol��С��0.8mol��˵�������¶�ƽ�����淴Ӧ�����ƶ��������¶�ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
��2���١���֪��H
2O��g��+3FeO��s��?Fe
3O
4��s��+H
2��g����H=a kJ/mol ����
2Fe
3O
4��s��=6FeO��s��+O
2 ��g����H=b kJ/mol ����
���ݸ�˹���ɣ�����2+���ã�2H
2O��g��=2H
2��g��+O
2��g�����ʡ�H=��2a+b��kJ/mol��
�ʴ�Ϊ����2a+b��kJ/mol��
�ڢ�FeOΪ���壬������С��Ӱ��ƽ���ƶ�����ʹ��ϸ����FeO���ôֿ���FeOʱH
2O��g����ת������ȣ�
�ʴ�Ϊ����ȣ�
��900��ʱƽ��ʱ��FeO��ת����Ϊ40%��ƽ��FeOת������Ϊ��n��FeO��=0.60mol��40%=0.24mol����
H
2O��g��+3FeO��s��?Fe
3O
4��s��+H
2��g��
��ʼ��mol����0.2 0.6 0 0
ת����mol����0.08 0.24 0.08 0.08
ƽ�⣨mol����0.12 0.36 0.08 0.08
��k=
=
=0.67
�𣺴��¶��¸÷�Ӧ��ƽ�ⳣ��Ϊ0.67��
��1000��ʱ��Ӧ���ʱ�900��죬����ƽ������ʱ��̣���ͼ1��֪�������¶�FeO��ת���ʽ��ͣ�ƽ�����淴Ӧ�����ƶ����������¶�H
2O��g��ת���ʽ��ͣ����������Ӱ��ת���ʣ�������Խϸ����Ӧ����Խ�죬��ͼ��Ϊ��
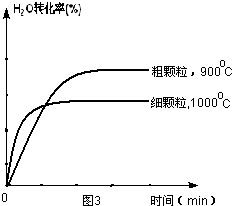
��
�ʴ�Ϊ��

��
���������⿼�黯��Ӧ���ʼ��㡢��Ӧ�ȼ��㡢ƽ�ⳣ�����㡢��ѧƽ����㼰Ӱ�����ء���ѧƽ��ͼ��ȣ���Ŀ�Ƚ��ۺϣ��Ѷ��еȣ����ضԻ���֪ʶ���̣���2����FeO������ˮ��ת����Ӱ��Ϊ�״��㣬ѧ�������������������ʵ�Ӱ������������жϣ�


 ��
�� ��
��





 ��ˮ��Һ�д���ƽ�⣺
��ˮ��Һ�д���ƽ�⣺ ����
���� ��CH3CH2OH����������Ӧʱ�����������ɵ��ǣ�������
��CH3CH2OH����������Ӧʱ�����������ɵ��ǣ�������
