
【题目】某化学活动小组设计如下图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质的成分。

(1)写出装置A中发生反应的化学方程式: 。
(2)装置B的主要作用是 。
(3)向C装置中通入一定量的氯气后,测得只生成一种气体(常温下为棕黄色,且为氯的氧化物)。可以确定的是C得到的固体最多含有三种物质,含有氯元素的盐只有一种,且含有NaHCO3,现对C中得到的固体成分进行猜想和验证。
① 提出合理猜想一定含有NaHCO3和 ;可能含有剩余的Na2CO3。
② 设计方案,进行成分检验。请完成实验步骤3、4以及预期现象和结论
限选实验试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、品红、稀盐酸。
1、实验步骤 | 2、预期现象和结论 |
3、步骤1:取C中的少量固体样品于试管中,加入蒸馏水至固体溶解,然后各取1~2mL所得溶液分别置于甲、乙两支试管中。 | 4、得到无色溶液 |
5、步骤2:向甲试管中加入过量的BaCl2溶液,静置 | 6、若溶液变浑浊,证明固体中含碳酸钠。 |
7、步骤3: | 8、 |
9、步骤4: | 10、 |
(4)完成C中反应的化学方程式:2Cl2+2Na2CO3+H2O= 。
【答案】(1)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)除去Cl2中混有的HCl气体
(3)①NaCl ②
实验步骤 | 预期现象和结论 |
步骤3:向甲中上层清液中滴入少量澄清石灰水 | 若上层清液变浑浊,证明固体中含有碳酸氢钠 |
步骤4:向乙试管中加入过量的稀HNO3,再滴入少量AgNO3溶液 | 若生成白色沉淀,证明固体中含有氯化钠 |
(4)2NaHCO3+NaCl+Cl2O(3分)
【解析】
试题分析:(1)A装置是制备氯气的,所以X试剂是浓盐酸,反应的化学方程式是MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(2)由于浓盐酸易挥发,所以生成的氯气中含有氯化氢,而氯化氢能和碳酸钠反应,所以需要除去氯气中的氯化氢。
(3)①由潮湿的氯气与Na2CO3发生的反应,结合已知信息来提出自己的假设。因产物中只有一种常温下为棕黄色的含氯氧化物气体,该含氯氧化物中氯元素的化合价应为正价,则产物中含氯元素的盐只能为NaCl。假设存在两种成分,为NaHCO3和NaCl;假设存在三种成分,应还有未完全反应的Na2CO3,即是NaHCO3、NaCl和Na2CO3;
②步骤2中向A试管中滴加适量BaCl2溶液,是检验产物中是否有Na2CO3。步骤3应是检验碳酸氢钠的,操作为向甲中上层清液中滴入少量澄清石灰水,若上层清液变浑浊,证明固体中含有碳酸氢钠;步骤4应是检验氯离子,应向乙试管中滴加过量的稀硝酸,再滴加AgNO3溶液,若溶液变浑浊,证明固体中含有NaCl。
(5)根据电子得失守恒可知,氧化产物中氯元素的化合价应该是+1价,所以其氧化产物是Cl2O,即C中反应生成的含氯氧化物为Cl2O,反应的方程式为2Cl2+2Na2CO3+H2O=2NaHCO3+NaCl+Cl2O。


科目:高中化学 来源: 题型:
【题目】21世纪是钛的世纪。下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
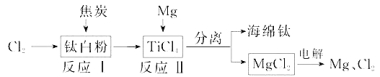
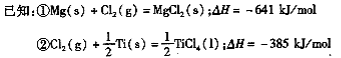
(1)钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的。TiO2+发生水解的离子方程式为 ;
(2)反应I在800~900℃下进行,还生成一种可燃性无色气体,该反应的化学方程式为: ;
(3)反应Ⅱ的热化学方程式为 ;
(4)该工艺流程中,可以循环使用的物质有 ;
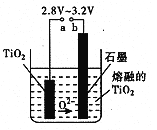
(5)在800 ~1000℃时电解TiO2也可制得海绵钛,装置如右图所示。图中b是电源的 极,阴极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现黑色和红色交替的现象,请写出此过程总的化学反应方程式____________________________________。
(2)甲和乙两个水浴作用不相同,其中甲的作用是______ _____。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们有水和________ _____ __ __。集气瓶中收集到的气体的主要成分是_____________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有乙酸,要除去该物质,可先在混合液中加入________(填字母序号),
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过__________(填实验操作名称)操作即可除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法正确的是( )
A. 18个纵横代表18个族,7个主族、8个副族
B. 短周期共有32种元素
C. 元素周期表共有七个横行代表七个周期
D. 第IA族全部是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质]
A、B、C、D、E是前四周期原子序数依次增大的五种元素。A元素原子的核外电子等于其电子层数;B元素基态原子有三个能级电子数相同;A和D可形成两种常见液态化合物甲、乙,其原子数之比分别为1:1,2:1;E元素原子的K、L层电子数之和等于其M、N层电子数之和。回答下列问题(涉及元素用相应化学符号表示):
(1)B、C、D三种元素中电负性最大的元素其基态原子的电子排布式为 。
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用 形象化描述。在B的基态原子中,核外存在 对自旋相反的电子。
(3)由E和D形成的晶胞如图1所示,晶体中E2+周围等距且最近的E2+有 个;ED的焰色反应为砖红色,许多金属或它们的化合物都可以发生焰色反应,焰色反应的原理是 。E和B可形成的晶体的晶胞结构与NaCl晶体的相似(如图2所示),但该晶体中含有的哑铃形B22-的存在,使晶胞沿一个方向拉长。晶体中E2+的配位数为_______________;该化合物的化学式为 。
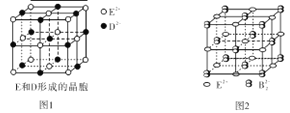
(4)用高能射线照射液态化合物乙时,一个乙分子能释放出一个电子,同时产生一种阳离子。
①释放出来的电子可以被若干乙分子形成的“网”捕获,乙分子间能形成“网”的原因是 。
②由乙分子释放出电子时产生的一种阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com