
| A、食盐 | B、食醋 | C、烧碱 | D、纯碱 |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
| A、氮气 | B、二氧化碳 |
| C、一氧化碳 | D、二氧化碳和氮气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA |
| B、标准状况下,2.24 L Cl2与过量NaOH溶液反应,转移的电子总数为0.2NA |
| C、1 mol/L的NaOH溶液中含Na+数目为NA |
| D、标准状况下,11.2 L CCl4中的C-Cl键数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C3H8 |
| B、C4H6 |
| C、C3H6 |
| D、C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、298K,反应③的△H3═+47.3 kJ?mol-1 |
| B、平衡时,其他条件不变,升高温度,反应①中正反应速率加快 |
| C、平衡时,其他条件不变,增大NO2浓度可增大反应③中SO2转化率 |
| D、反应③中,每有1mol O=O键断裂,同时生成2molSO3,则该反应达平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
131 53 |
| A、25 | B、78 |
| C、103 | D、184 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在NaH中的氢离子半径比锂离子半径大 |
| B、在NaH中的氢离子的电子层排布与氦原子不相同 |
| C、NaH跟水反应后溶液呈酸性 |
| D、NaH中的氢离子被还原成氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
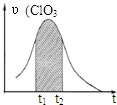 KClO3和KHSO3能发生反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.图为用ClO3-在单位时间内物质的量浓度变化表示的该反应υ-t图.下列说法正确的( )
KClO3和KHSO3能发生反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.图为用ClO3-在单位时间内物质的量浓度变化表示的该反应υ-t图.下列说法正确的( )| A、反应开始时速率增大可能是c(H+)所致 |
| B、纵坐标为υ(Cl-)的υ-t曲线与图中曲线不能完全重合 |
| C、后期速率υ下降的主要原因是反应向逆反应方向进行 |
| D、图中阴影“面积”可以表示t1-t2时间内c(Cl-)增加量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com