
 H2↑+Cl2↑+2OH-; 电解一段时间后两极共收集到标准状况下的气体1.12L,物质的量为0.05mol,依据离子方程式计算得到生成氢氧根离子物质的量为0.05mol,c(OH-)=
H2↑+Cl2↑+2OH-; 电解一段时间后两极共收集到标准状况下的气体1.12L,物质的量为0.05mol,依据离子方程式计算得到生成氢氧根离子物质的量为0.05mol,c(OH-)=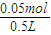 =0.1mol/L;氢离子浓度为10-13mol/L,pH=13,
=0.1mol/L;氢离子浓度为10-13mol/L,pH=13, H2↑+Cl2↑+2OH-;13;
H2↑+Cl2↑+2OH-;13;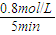 =0.16mol/L?min,
=0.16mol/L?min,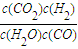 =
=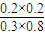 =0.17,
=0.17,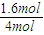 ×100%=40%,实验2中CO的转化率为
×100%=40%,实验2中CO的转化率为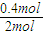 ×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热,
×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热,

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2012-2013学年河北省邯郸市高三第二次模拟考试理综化学试卷(解析版) 题型:简答题
硼及其化合物在耐髙温合金工业、催化剂制造、髙能燃料等方面应用广泛。
(1)氮化硼是一种耐高温材料,巳知相关反应的热化学方程式如下:
2B(s)+N2(g)= 2BN(s) ΔH=a kJ • mol-1
B2H6 (g)=2B(s) + 3H2 (g) ΔH =b kJ • mol-1
N2 (g) + 3H2
(g) 2NH3 (g) ΔH =c kJ• mol-1
2NH3 (g) ΔH =c kJ• mol-1
①反应B2H6(g)+2NH3(g)=2BN(s) +6H2(g) ΔH = (用含a、b、c 的代数式表示)kJ ·mol-1。
②B2H6是一种髙能燃料,写出其与Cl2反应生成两种氯化物的化学方程式: 。
(2)硼的一些化合物的独特性质日益受到人们的关注。
①最近美国化学家杰西·萨巴蒂尼发现由碳化硼制作的绿色焰火比传统焰火(硝酸钡)更安全,碳化硼中硼的质量分数为78. 6%,则碳化硼的化学式为 。
②近年来人们将LiBH4和LiNH2球磨化合可形成新的化合物 Li3BN2H8和Li4BN3 H10,Li3BN2H8球磨是按物质的量之比n(LiNH2) : n(LiBH4) = 2 : 1加热球磨形成的,反应过程中的X衍射图谱如图所示。

Li3BN2H8在大于250℃时分解的化学方程式为 ,Li3BN2H8与Li4BN3H10 的物质的量相同时,充分分解,放出等量的H2,Li4BN3 H10分解时还会产生固体Li2NH和另一种气体,该气体是 。
(3)直接硼氢化物燃料电池的原理如图,负极的电极反应式为 。电池总反应的离子方程式为 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com