
| A. | 10mL 18mol/L 浓硫酸与足量铜加热充分反应,其中有 0.09NA 个 H2SO4 体现 了氧化性 | |
| B. | 将 5.6g 铁在 3.36LCl2 中点燃,二者一定能恰好完全反应 | |
| C. | 100mL 1mol/L 硫酸溶液中,有 0.1mol H2SO4分子 | |
| D. | 标准状况下,22.4 L CO2和 CO 混合气体中含有的碳原 子数约为 NA |
分析 A.铜与浓硫酸反应,与稀硫酸不反应;
B.气体状况未知;
C.硫酸为强电解质,水溶液中完全电离;
D.求出混合气体的物质的量,然后根据二氧化碳和CO中均含1个碳原子来分析.
解答 解:A.随着反应进行浓硫酸浓度降低,稀硫酸与铜不反应,所以稀释氧化性的硫酸分子个数小于 0.09NA 个,故A错误;
B.气体状况未知,无法计算氯气的物质的量,故B错误;
C.硫酸为强电解质,水溶液中完全电离,所以硫酸溶液中不存在硫酸分子,故C错误;
D.标况下22.4L混合气体的物质的量为1mol,而二氧化碳和CO中均含1个碳原子,故1mol二氧化碳和CO的混合物中含有的碳原子为NA个,与两者的比例无关,故D正确.
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意浓度对反应的影响,注意气体摩尔体积使用条件和对象,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 洗净的锥形瓶和容量瓶可以放进烘箱中烘干 | |
| B. | 中和热测定实验的量热计中有少量水不影响测定结果 | |
| C. | 中和滴定实验中,用待装溶液润洗滴定管以减小实验误差 | |
| D. | 硫酸铜结晶水含量测定实验中至少用托盘天平称量3次 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
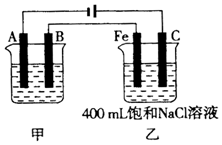 如图为相互串联的甲、乙两电解池.
如图为相互串联的甲、乙两电解池.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO4═2Na++SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | NaOH═Na++O2-+H+ | D. | H2SO4═H22++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在食盐中添加适量的碘酸钾 | |
| B. | 用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的 | |
| C. | 一些工业用燃料,如苏丹红等,对人体无毒害作用,也可用作食用色素 | |
| D. | 研究高效低毒的农药,降低蔬菜的农药残留量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量金属钠保存在水里 | |
| B. | 澄清石灰水需盛放在用橡皮塞塞紧的试剂瓶中 | |
| C. | 为了防止Fe2+被氧化,可在盛FeSO4溶液的试剂瓶中加少量铁粉 | |
| D. | 新制氯水通常保存在棕色试剂瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com