
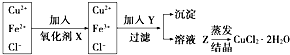
 工业上制取纯净的CuCl2•2H2O的主要过程是:
工业上制取纯净的CuCl2•2H2O的主要过程是:分析 工业上制取纯净的CuCl2•2H2O的主要过程:将粗氧化铜(含少量Fe)溶解于稀盐酸中,氧化铜和盐酸反应生成氯化铜,铁和盐酸反应生成氯化亚铁,过滤,滤液中含有亚铁离子、铜离子、氯离子,加入氧化剂将亚铁离子氧化成铁离子,然后加入Y调节溶液的pH,将铁离子转化成氢氧化铁沉淀除去,得到的溶液乙为氯化铜溶液,然后在持续通入HCl气体并不断搅拌条件下蒸发溶液乙获得氯化铜晶体.
(1)依据流程图可知实验目的是制备氯化铜晶体,需要除去亚铁离子,加入的X为氧化剂,但不能引入新的杂质;
(2)Y物质应调节溶液的酸性,调节溶液PH时铁离子全部沉淀,铜离子不能沉淀且不能引入新的杂质离子;
(3)氯化铜水溶液蒸发浓缩,铜离子水解,生成的氯化氢挥发,加热促进水解正向进行,得到氢氧化铜,实验需要在氯化氢气流中蒸发析出晶体.
解答 解:工业上制取纯净的CuCl2•2H2O的主要过程:将粗氧化铜(含少量Fe)溶解于稀盐酸中,氧化铜和盐酸反应生成氯化铜,铁和盐酸反应生成氯化亚铁,过滤,滤液中含有亚铁离子、铜离子、氯离子,加入氧化剂将亚铁离子氧化成铁离子,然后加入Y调节溶液的pH,将铁离子转化成氢氧化铁沉淀除去,得到的溶液乙为氯化铜溶液,然后在持续通入HCl气体并不断搅拌条件下蒸发溶液乙获得氯化铜晶体.
(1)依据流程图可知实验目的是制备氯化铜晶体,需要除去亚铁离子,加入的X为氧化剂,但不能引入新的杂质,通入氯气氧化亚铁离子为铁离子,反应的离子方程式为:Cl2+2Fe2+=2Fe3++2Cl-,若X是过氧化氢溶液,酸性溶液中也可以氧化亚铁离子为铁离子且不引入新的杂质,反应的离子方程式为:2H++H2O2+2Fe2+=2Fe3++2H2O;
故答案为:Cl2(H2O2);Cl2+2Fe2+=2Fe3++2Cl-(2H++H2O2+2Fe2+=2Fe3++2H2O);
(2)Y物质应调节溶液的酸性,调节溶液PH时铁离子全部沉淀,铜离子不能沉淀且不能引入新的杂质离子,实验需要加入和酸反应的固体物质CuO或Cu(OH)2,已知Cu2+、Fe2+在pH为4~5时不水解,而Fe3+几乎完全水解而沉淀,调节溶液PH值4--5,使铁离子完全沉淀;
故答案为:调节溶液的酸性,使PH为4~5,且不引入新杂质;CuO或Cu(OH)2 ;
(3)氯化铜水溶液蒸发浓缩,铜离子水解,CuCl2+H2O?Cu(OH)2+2HCl,生成的氯化氢挥发,加热促进水解正向进行,得到氢氧化铜,所以实验需要在氯化氢气流中蒸发,抑制水解反应进行,析出得到氯化铜晶体;
故答案为:通入HCl气体(或加入盐酸),并不断搅拌且不能蒸干.
点评 本题考查了物质制备实验方案的分析判断,实验操作过程的注意问题,除杂不能引入新的杂质是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,相同体积的物质,其物质的量一定相等 | |
| B. | 一氧化碳气体和氮气,若体积相等,则质量一定相等 | |
| C. | 1L一氧化碳气体一定比1L氧气的质量小 | |
| D. | 任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
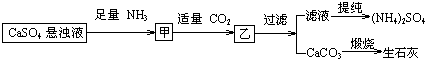
| A. | 通入CO2和NH3顺序可以颠倒 | |
| B. | 通入的NH3必须过量 | |
| C. | CO2可被循环使用 | |
| D. | 生成1mol(NH4)2SO4至少消耗2 mol NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
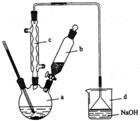 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 对叔丁基苯酚
对叔丁基苯酚 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚.实验步骤如下:反应物和产物的相关数据列表如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚.实验步骤如下:反应物和产物的相关数据列表如下: .该反应过于激烈,放出大量热,常使实验的产率降低,可能的原因是由于叔丁基氯挥发导致产率降低.
.该反应过于激烈,放出大量热,常使实验的产率降低,可能的原因是由于叔丁基氯挥发导致产率降低.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
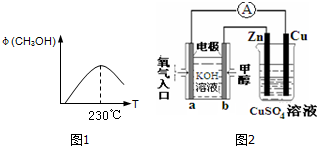
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |

| 实验次数 温度 | 起始温度t1/℃ | 终止温度t2/℃ | 平均温度差(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com