
【题目】下列关于硅酸的叙述,错误的是( )
A. 硅酸是一种很弱的酸
B. 硅酸可由二氧化硅与水反应制得
C. 硅酸不稳定,加热脱水会生成二氧化硅
D. 硅酸可以由可溶性硅酸盐与盐酸反应制得
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】在500 g含1.17 g NaCl和0.84 g NaF的溶液中,滴加过量的AgNO3溶液,静置,过滤,洗涤,称重得到2.87 g固体,由此可以得出的正确结论是( )
A. 氯离子只有一部分参加反应
B. 氟离子只有一部分参加反应
C. 氟化钠与AgNO3在溶液中无沉淀生成
D. 氟化银难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝制品比铁制品在空气中不易被锈蚀,原因是( )
A. 铝的金属性比铁弱B. 铝在空气中易与氧气形成一层致密的氧化膜
C. 铝的密度比铁的密度小D. 铝不能与氧气发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,0.1mol/L的二元酸H2A溶液中,溶液体系可能存在的含A粒子(H2A、HA﹣、A2﹣)所占物质的量分数随pH变化的关系如图所示,下列说法正确的是( )
A.H2A的电离方程式为:H2AH++HA﹣
B.pH=5时,在NaHA和Na2A的混合溶液中:c(HA﹣):c(A2﹣)=1:100
C.等物质的量浓度的NaHA和Na2A溶液等体积混合,离子浓度大小关系为c(Na+)>c(HA﹣)>c(A2﹣)
D.Na2A溶液必存在c(OH﹣)=c(H+)+c(HA﹣)+2c(H2A),各粒子浓度均大于0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的说法正确的是( )
A.1mol ![]() 能与4molNaOH充分反应
能与4molNaOH充分反应
B.![]() 系统命名法为3﹣丁烯
系统命名法为3﹣丁烯
C.![]() 的碳原子都在一个平面内,且它的二氯代物为3种
的碳原子都在一个平面内,且它的二氯代物为3种
D.1mol ![]() 可以与4molH2发生加成
可以与4molH2发生加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应(表示物质均为反应物)中,反应刚开始时,放出氢气速率最大的是( )
编号 | 金属(块状) | 酸的浓度及体积 | 反应温度(℃) |
A | 0.2mol Mg | 10 mL2.5 mol·L-1硫酸 | 60 |
B | 0.2mol Mg | 40 mL3 mol·L-1盐酸 | 60 |
C | 0.2mol Fe | 50 mL5 mol·L-1盐酸 | 60 |
D | 0.2mol Mg | 20 mL2.5 mol·L-1硫酸 | 50 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( ) 
选项 | 实验试剂 | 实验结论 | ||
A | a.稀硫酸 | b.碳酸氢钠 | c.硅酸钠溶液 | 酸性:硫酸>碳酸>硅酸 |
B | a.稀盐酸 | b.二氧化锰 | c.溴化钠溶液 | 氧化性:MnO2>Cl2>Br2 |
C | d.小苏打 | e.苏打 | f.石灰水 | 热稳定性:苏打>小苏打 |
D | d.氯化钠 | e.氯化铵 | f.硝酸银溶液 | 沸点:氯化钠>氯化铵 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各图的叙述正确的是( )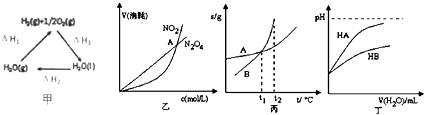
A.甲中△H1=﹣(△H2+△H3)
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g)═N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A,B两物质的溶解度随温度变化情况,将tl℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA,HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于等物质的量浓度的NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛是深受关注的有机化合物.甲醛含量的测定有多种方法,例如:在调至中性的亚硫酸钠溶液中加入甲醛水溶液,经充分反应后,产生的氢氧化钠的物质的量与甲醛的物质的量相等,然后用已知浓度的硫酸滴定氢氧化钠.
完成下列填空:
(1)将4.00mL甲醛水溶液加入到经调至中性的亚硫酸钠溶液中,充分反应后,用浓度为1.100mol/L的硫酸滴定,至终点时耗用硫酸20.00mL.甲醛水溶液的浓度为;上述滴定中,若滴定管规格为50mL,甲醛水溶液取样不能超过mL.
(2)甲醛和新制氢氧化铜的反应显示了甲醛的还原性,发生反应的化学方程式通常表示如下:HCHO+2Cu(OH)2![]() HCOOH+Cu2O↓+2H2O,每1mol甲醛参加反应转移的电子数为个.甲醛中的碳的杂化方式为 . (填sp、sp2、sp3)
HCOOH+Cu2O↓+2H2O,每1mol甲醛参加反应转移的电子数为个.甲醛中的碳的杂化方式为 . (填sp、sp2、sp3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com