
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:阅读理解


| 1 |
| 2 |
| 1 |
| 2 |
| YO2 | YO3 | |
| 空气 | 94%-95% | 5%-6% |
| 氧气 | 97%-98% | 2%-3% |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

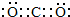
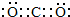
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第19~26期 总第175~182期 人教课标版 题型:022
氮的化合物在某些领域中扮演着重要的角色,其中硝酸是工业的三大强酸之一.
(1)试从原料的利用率和环境保护两个角度分析,
溶解等量的金属铜,用浓硝酸好,还是用稀硝酸好?写出反应的化学方程式并做简要解释:________________.
(2)金属与不同浓度的硝酸反应时,往往生成多种不同价态的还原产物.下图是各种不同密度的硝酸与铁反应时(相同温度)的还原产物分布图.
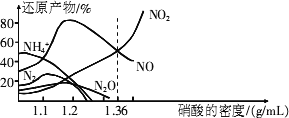
①某硝酸试剂瓶的标签注明:密度:
1.26 g/mL,质量分数:50.0%.若取该试剂10 mL配成1000 mL溶液,所得溶液的物质的量浓度为________;②当硝酸溶液的密度为
1.36 g/mL时,下列化学方程式中能较准确地表达Fe与过量硝酸反应的是________ (填序号).a.2Fe+10HNO3![]() 2Fe(NO3)3+NO↑+3NO2↑+5H2O
2Fe(NO3)3+NO↑+3NO2↑+5H2O
b.4Fe+18HNO3![]() 4Fe(NO3)3+3NO↑+3NO2↑+9H2O
4Fe(NO3)3+3NO↑+3NO2↑+9H2O
c.2Fe+6HNO3![]() 2Fe(NO3)2+NO↑+NO2↑+3H2O
2Fe(NO3)2+NO↑+NO2↑+3H2O
(3)三聚氰胺[C3N3(NH2)3]是一种重要的有机化工原料,因其含氮量高达66.7%而被不法商家用作食品添加剂,以提升食品检测中的蛋白质含量(以氮元素的质量分数N%表示).某品牌奶粉中N%为1.9%,若在100 g该奶粉中加入10 g三聚氰胺,则N%提高为原来的________倍(取整数).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com