
分析 根据C=$\frac{n}{V}$,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差.
解答 解:(1)生锈的砝码质量偏大,而m物=m砝+m游,故称量出的药品的质量偏重,则配制出的溶液的浓度偏大,
故答案为:偏高;
(2)定容摇匀时,液面下降又加水,导致所配溶液体积v偏大,所配溶液浓度偏低,
故答案为:偏低;
(3)定容时俯视读取刻度,导致所配溶液体积V偏小,所配溶液浓度偏高,
故答案为:偏高;
(4)容量瓶是定容仪器,使用时,用蒸馏水洗净后未干燥,不会影响结果,
故答案为:不变;
(5)烧杯中氯化钠溶液移入容量瓶后,没有洗涤烧杯和转移洗涤液,导致溶质的物质的量偏小,溶液的浓度偏低,
故答案为:偏低.
点评 本题考查了配制一定物质的量浓度溶液时的误差分析,要从不当的操作对溶液的体积或溶质的质量的影响来着手分析,难度不大.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:选择题
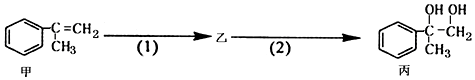
| A. | 物质丙能与氢氧化钠溶液反应 | |
| B. | 甲和丙均可使酸性KMnO4溶液褪色 | |
| C. | 反应(2)属于取代反应 | |
| D. | 步骤(2)产物中可能含有未反应的甲,可用溴水检验是否含甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 木材纤维和土豆淀粉遇碘水均显蓝色 | |
| B. | 食用油反复加热会产生稠环芳烃等有害物质 | |
| C. | 误食铜、铅或汞等重金属盐中毒后应立即服用大量的牛奶 | |
| D. | 食用花生油和鸡蛋清都能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35L | B. | 30L | C. | 25L | D. | 20 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
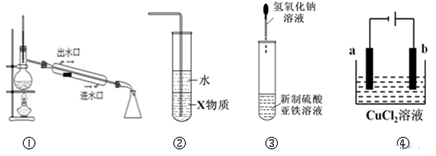
| A. | 实验室用装置①蒸馏石油 | |
| B. | 装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| C. | 装置③可用于制备氢氧化亚铁并观察其颜色 | |
| D. | 装置④是电解精炼铜,b极为粗铜,发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
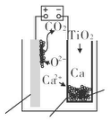 研究发现,可以用石墨作阳极、钛网作阴极、熔融的 CaF2-CaO 作电解质,利用如图 所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中,正确的是( )
研究发现,可以用石墨作阳极、钛网作阴极、熔融的 CaF2-CaO 作电解质,利用如图 所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中,正确的是( )| A. | 由 TiO2 制得 1 mol 金属 Ti,理论上外电路通过 2 mol 电子 | |
| B. | 阳极的电极反应式为 C+2O2--4e-═CO2↑ | |
| C. | 在制备金属钛前后,整套装置中 CaO 的总量减少 | |
| D. | 若用铅蓄电池作该装置的供电电源,“+”接线柱应连接 Pb 电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
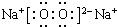 ,其中含有的化学键是离子键、共价键.
,其中含有的化学键是离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该物质是有机物 | B. | 该分子中含有9个σ键和10个π键 | ||
| C. | 该分子可发生加成反应 | D. | 该分子中所有原子在同一直线上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com