
”¾ĢāÄæ”æµē×Ó¹¤Ņµ³£ÓĆ30%µÄFeCl3ČÜŅŗøÆŹ“·óŌŚ¾ųŌµ°åÉĻµÄĶ²£¬ÖĘŌģÓ”Ė¢µēĀ·°å”£
£Ø1£©¼ģŃéČÜŅŗÖŠFe3+“ęŌŚµÄŹŌ¼ĮŹĒ________£¬Ö¤Ć÷Fe3+“ęŌŚµÄĻÖĻóŹĒ________”£
£Ø2£©Š“³öFeCl3ČÜŅŗÓė½šŹōĶ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ________”£
£Ø3£©Ä³¹¤³ĢŹ¦ĪŖĮĖ“ÓŹ¹ÓĆ¹żµÄøÆŹ“·ĻŅŗÖŠ»ŲŹÕĶ£¬²¢ÖŲŠĀ»ńµĆ“æ¾»µÄFeCl3ČÜŅŗ£¬×¼±ø²ÉÓĆĻĀĮŠ²½Öč£ŗ

ĒėŠ“³öÉĻŹöŹµŃéÖŠ¼ÓČė»ņÉś³ÉµÄÓŠ¹ŲĪļÖŹµÄ»ÆѧŹ½”£
¢Ł________£¬¢Ü________”£
£Ø4£©ŅŖÖ¤Ć÷ijČÜŅŗÖŠ²»ŗ¬Fe3+¶ųæÉÄÜŗ¬ÓŠFe2+£¬½ųŠŠČēĻĀŹµŃé²Ł×÷Ź±µÄ×ī¼ŃĖ³ŠņĪŖ________”£
¢Ł¼ÓČė×ćĮæĀČĖ®¢Ś¼ÓČė×ćĮæKMnO4ČÜŅŗ¢Ū¼ÓČėÉŁĮæKSCNČÜŅŗ
A£®¢Ł¢Ū B£®¢Ū¢Ś C£®¢Ū¢Ł D£®¢Ł¢Ś¢Ū
£Ø5£©Š“³öĻņ¢Ś¢ŻµÄ»ģŗĻŅŗÖŠĶØČė¢ŽµÄĄė×Ó·½³ĢŹ½£ŗ________”£
”¾“š°ø”æ KSCN ČÜŅŗ±ä³ÉŃŖŗģÉ« 2Fe3£«£«Cu![]() 2Fe2£«£«Cu2£« Fe HCl C 2Fe2£«£«Cl2
2Fe2£«£«Cu2£« Fe HCl C 2Fe2£«£«Cl2![]() 2Fe3£«£«2Cl£
2Fe3£«£«2Cl£
”¾½āĪö”æ£Ø1£©±¾Ģāæ¼²éFe3£«¼ģŃ飬¼ģŃéFe3£«³£ÓĆKSCNČÜŅŗ£¬Čē¹ūČÜŅŗ±äĪŖŃŖŗģÉ«£¬ĖµĆ÷ŗ¬ÓŠFe3£«£¬·“Ö®²»ŗ¬ÓŠ£»£Ø2£©±¾Ģāæ¼²éCuŗĶFe3£«·“Ó¦£¬Ąė×Ó·“Ó¦·½³ĢŹ½ĪŖCu£«2Fe3£«=2Fe2£«£«Cu2£«£»£Ø3£©±¾Ģāæ¼²é»Æѧ¹¤ŅÕĮ÷³Ģ£¬±¾ŹµŃéÄæµÄŹĒ»ŲŹÕĶŗĶÖĘČ”“æ¾»µÄFeCl3£¬Ļņ·ĻŅŗÖŠ¼ÓČė¹żĮæµÄĢśŠ¼£¬Č»ŗó¹żĀĖ£¬ĀĖŅŗĪŖFeCl2£¬ĀĖŌüĪŖCuŗĶFe£¬ŅņĪŖĢśÄÜÓėŃĪĖį·“Ó¦£¬ĶŗĶŃĪĖį²»·“Ó¦£¬Ņņ“ĖĀĖŌü¢ŪÖŠ¼ÓČė¹żĮæµÄŃĪĖį£¬¹żĀĖ£¬µĆµ½½šŹōĶ£¬Į½ÖÖĀĖŅŗŗĻ²¢£¬ĶØČėĀČĘų£¬°ŃFe2£«Ńõ»Æ³ÉFe3£«£»£Ø4£©±¾Ģāæ¼²éĄė×Ó¼ģŃ飬¼ģŃéijČÜŅŗÖŠ²»ŗ¬Fe3£«£¬ŗ¬Fe2£«£¬Ó¦ĻČ¼ÓKSCNČÜŅŗ£¬ČÜŅŗ²»±äŗģ£¬ĖµĆ÷²»ŗ¬Fe3£«£¬ŌŁ¼ÓČėŃõ»Æ¼Į£¬ČÜŅŗ±äŗģ£¬ĖµĆ÷ŌČÜŅŗÖŠŗ¬Fe2£«£¬²»ŗ¬Fe3£«£¬Ńõ»Æ¼Į²»ÄÜŹĒĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£¬ŅņĪŖøßĆĢĖį¼ŲČÜŅŗÄÜŃõ»ÆKSCN£¬¹ŹŃ”ĻīCÕżČ·£»£Ø5£©±¾Ģāæ¼²éĄė×Ó·“Ó¦·½³ĢŹ½µÄŹéŠ“£¬¢ŽĪŖĀČĘų£¬·¢ÉśµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ2Fe2£«£«Cl2=2Fe3£«£«2Cl£”£


 ³õ֊ѧŅµæ¼ŹŌµ¼ÓėĮ·ĻµĮŠ“š°ø
³õ֊ѧŅµæ¼ŹŌµ¼ÓėĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNOĖäŹĒ“óĘųĪŪČ¾Īļ£¬µ«ŃŠ¾æ±ķĆ÷ÉŁĮæNOŌŚČĖĢåÄŚæɲĪÓėÉń¾ĻµĶ³µÄµ÷æŲ”£
£Ø1£©ŹµŃéŹŅÓĆ½šŹōĶŗĶĻ”ĻõĖįÖĘČ”NOµÄ»Æѧ·½³ĢŹ½ĪŖ__________”£
£Ø2£©Ä³Ķ¬Ń§Éč¼ĘĮĖČēĻĀĶ¼ĖłŹ¾×°ÖĆ£¬ŃŠ¾æĶĖæÓėĻ”ĻõĖį·“Ӧɜ³ÉµÄĘųĢåČ·ŹµŹĒNO”£
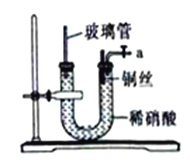
¢Ł·“Ó¦æŖŹ¼ŗó,æÉŅŌ¹Ū²ģµ½µÄĻÖĻóŹĒµ¼¹Üa“¦²śÉśĪŽÉ«ĘųĢ唢_______”£
¢Ś²£Į§¹ÜµÄ×÷ÓĆŹĒ_________”£
¢ŪČōŠčŹ¹·“Ó¦Ķ£Ö¹.æɲÉČ”µÄ²Ł×÷ŹĒ________”£
£Ø3£©ČēŅŖŌŚÉĻĶ¼a¹Ü“¦Į¬½ÓŹÕ¼ÆNOĘųĢåµÄ×°ÖĆ£¬ŗĻĄķµÄŹĒ______(Ģī×ÖÄø)”£
£Ø4£©¹¤ŅµÉĻĄūÓĆ°±ĘųŗĶŃõĘųÖĘČ”NOµÄ·½·ØŹĒ(Ģī»Æѧ·½³ĢŹ½)__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ²Īæ¼ČēĶ¼ŗĶÓŠ¹ŲŅŖĒó»Ų“šĪŹĢā£ŗ 
£Ø1£©¼×“¼ÖŹ×Ó½»»»Ä¤Č¼ĮĻµē³ŲÖŠ½«¼×“¼ÕōĘų×Ŗ»ÆĪŖĒāĘųµÄŅ»ÖÖŌĄķŹĒCH3OH£Øg£©ŗĶH2O£Øg£©·“Ӧɜ³ÉCO2ŗĶH2 £® Ķ¼1ŹĒøĆ¹ż³ĢÖŠÄÜĮæ±ä»ÆŹ¾ŅāĶ¼£¬ČōŌŚ·“Ó¦ĢåĻµÖŠ¼ÓČė“߻ƼĮ£¬·“Ó¦ĖŁĀŹŌö“ó£¬Õż·“Ó¦»ī»ÆÄÜ aµÄ±ä»ÆŹĒ£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±”¢”°²»±ä”±£©£¬·“Ó¦ČČ”÷HµÄ±ä»ÆŹĒ£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±”¢”°²»±ä”±£©£®
£Ø2£©ŅŌCH3OHČ¼ĮĻµē³ŲĪŖµēŌ“µē½ā·ØÖĘČ”ClO2 £® ¶žŃõ»ÆĀČ£ØClO2£©ĪŖŅ»ÖÖ»ĘĀĢÉ«ĘųĢ壬ŹĒ¹ś¼ŹÉĻ¹«ČĻµÄøߊ§”¢¹ćĘ×”¢æģĖŁ”¢°²Č«µÄɱ¾śĻū¶¾¼Į£® ¢ŁCH3OHČ¼ĮĻµē³Ų·Åµē¹ż³ĢÖŠ£¬ĶØČėO2µÄµē¼«ø½½üČÜŅŗµÄpH£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±”¢”°²»±ä”±£©£®øŗ¼«·“Ó¦Ź½ĪŖ £®
¢ŚĶ¼2ÖŠµē½ā³ŲÓĆŹÆÄ«×÷µē¼«£¬ŌŚŅ»¶ØĢõ¼žĻĀµē½ā±„ŗĶŹ³ŃĪĖ®ÖĘČ” ClO2 £® Ńō¼«²śÉś ClO2µÄ·“Ó¦Ź½ĪŖ £®
¢Ūµē½āŅ»¶ĪŹ±¼ä£¬“ÓŅõ¼«“¦ŹÕ¼Æµ½µÄĘųĢå±ČŃō¼«“¦ŹÕ¼Æµ½ĘųĢå¶ą 6.72LŹ±£Ø±ź×¼×“æö£¬ŗöĀŌÉś³ÉµÄĘųĢåČܽā£©£¬Ķ£Ö¹µē½ā£¬ĶعżŃōĄė×Ó½»»»Ä¤µÄŃōĄė×ÓĪŖmol£®
£Ø3£©Ķ¼2ÖŠµē½ā³ŲøÄĪŖÓĆŹÆÄ«×÷µē¼«£¬ŌŚŅ»¶ØĢõ¼žĻĀµē½ā0.05molL©1µÄĮņĖįĶČÜŅŗ200mL£¬µ±Į½¼«²śÉśµÄĘųĢåĢå»żĻąĶ¬Ź±£¬ ¢Ł·¢Éśµē½āµÄ×Ü·“Ó¦·½³ĢŹ½ĪŖ
¢ŚČōµē½āŗóČÜŅŗµÄĢå»ż»¹ŹĒ200mL£¬ČÜŅŗµÄpH=
¢Ūµē½āŗó¼ÓČėĻĀĮŠ¹ĢĢåĪļÖŹæÉŹ¹ČÜŅŗ»Öø“µ½µē½āĒ°
A CuO B Cu £ØOH£©2C CuCO3D CuSO4 £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒ³£¼ūŌŖĖŲµÄĪļÖŹ×Ŗ»Æ¹ŲĻµĶ¼(²æ·ÖĪļÖŹ±»Ź”ĀŌ)£¬A.DŹĒ³£¼ū½šŹōµ„ÖŹ£¬CŹĒÖŲŅŖµÄÄĶ»š²ÄĮĻ£¬GµÄĖ®ČÜŅŗÖŠµĪ¼ÓKSCN³ŹŗģÉ«”£F ĪŖĮ½ÖÖŌŖĖŲ×é³ÉµÄ“Ģ¼¤ŠŌĘųĢ壬ŹĒ³£¼ūµÄ“óĘųĪŪČ¾Īļ£¬ĘäĮ½ÖÖŌŖĖŲµÄÖŹĮæ±ČĪŖ1£ŗ1.ÉŁĮæFĶØČėEČÜŅŗÖŠ²śÉś°×É«³ĮµķH”£MŹĒŗģŗÖÉ«¹ĢĢ唣

£Ø1£©Š“³öĻĀĮŠĪļÖŹµÄ»ÆѧŹ½£ŗA____________”¢E___________”¢F___________”¢G___________;
£Ø2£©Š“³öĻĀĮŠ·“Ó¦µÄ·“Ó¦·½³ĢŹ½£ØÄÜŠ“Ąė×Ó·½³ĢŹ½µÄ±ŲŠėŠ“Ąė×Ó·½³ĢŹ½£©
·“Ó¦¢Ł____________________________________£»
·“Ó¦¢Ś____________________________________£»
·“Ó¦¢Ż____________________________________£»
£Ø3£©Kµ½MÓŠĮ½ÖÖ·½Ź½æÉŅŌŹµĻÖ
¢Ł¼ÓČėĒāŃõ»ÆÄĘ²¢³Ø·ÅÓŚæÕĘųÖŠ£¬“ĖŹ±æɹŪ²ģµ½µÄĻÖĻóŹĒ_________________________________£»
¢ŚÖ»¼ÓČėŅ»ÖÖ¹ĢĢåĪļÖŹLÖ±½ÓŹµĻÖ£¬ŌņLµÄ»ÆѧŹ½ĪŖ£ŗ__________£¬Čō°“n(K)£ŗn(L)=1:1¼ÓČė£¬Ąė×Ó·½³ĢŹ½ĪŖ____________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ±ä»ÆÖŠ£¬ĘųĢå±»»¹ŌµÄŹĒ
A. CO2Ź¹Na2O2±ä°×É« B. Cl2Ź¹FeCl2ČÜŅŗ±ä»ĘÉ«
C. H2Ź¹×ĘČȵÄCuO·ŪÄ©±äŗģÉ« D. CO2ÄÜŹ¹ŹÆ»ŅĖ®±ä»ė×Ē
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠŅ»¶ØĮæŗ¬ÓŠNa2OŌÓÖŹµÄNa2O2ŹŌŃł£¬ÓĆČēĶ¼µÄŹµŃé×°ÖĆ²ā¶ØNa2O2ŹŌŃłµÄ“æ¶Č”££Øæɹ©Ń”ÓƵķ“Ó¦ĪļÖ»ÓŠCaCO3¹ĢĢ唢6 mol”¤L-1ŃĪĖį”¢6 mol”¤L-1ĮņĖįŗĶÕōĮóĖ®£©

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©×°ÖĆAÖŠŅŗĢåŹŌ¼ĮŃ”ÓĆ________
£Ø2£©×°ÖĆBµÄ×÷ÓĆŹĒ_________________£¬×°ÖĆCµÄ×÷ÓĆŹĒ_________________________£¬×°ÖĆEÖŠ¼īŹÆ»ŅµÄ×÷ÓĆŹĒ______________________________________________”£
£Ø3£©×°ÖĆDÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_________________________”£
£Ø4£©ČōæŖŹ¼Ź±²āµĆѳʷµÄÖŹĮæĪŖ2.0 g£¬·“Ó¦½įŹųŗó²āµĆĘųĢåĢå»żĪŖ224 mL£Ø±ź×¼×“æö£©£¬ŌņNa2O2ŹŌŃłµÄ“æ¶ČĪŖ_____________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ£Ø £©
A.NaOHČÜŅŗÖŠµĪČėCuSO4ČÜŅŗOH©+Cu2+=Cu£ØOH£©2”ż
B.ŅŅČ©·¢ÉśŅų¾µ·“Ó¦CH3CHO+2[Ag£ØNH3£©2]++2OH© ![]() CH3COO©+NH4+2Ag”ż+3NH3+H2O
CH3COO©+NH4+2Ag”ż+3NH3+H2O
C.“×ĖįÓėĢ¼ĖįÄĘČÜŅŗ·“Ó¦CO32©+2H+=H2O+CO2”ü
D.äåŅŅĶéÖŠµĪČėAgNO3ČÜŅŗAg++Br©=AgBr”ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪļÖŹA-KÓŠČēĶ¼ĖłŹ¾×Ŗ»Æ¹ŲĻµ£¬ĘäÖŠĘųĢåD”¢EĪŖµ„ÖŹ£¬ŹŌ»Ų“šĻĀĮŠĪŹĢā:
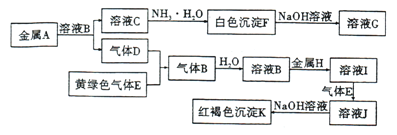
(1)Š“³öĻĀĮŠĪļÖŹµÄ»ÆѧŹ½:ĘųĢåDŹĒ________,HŹĒ________.
(2)Š“³ö·“Ó¦”°I![]() J”±µÄĄė×Ó·½³ĢŹ½:__________
J”±µÄĄė×Ó·½³ĢŹ½:__________
(3)Š“³ö·“Ó¦”°F![]() G" µÄĄė×Ó·½³ĢŹ½:____________
G" µÄĄė×Ó·½³ĢŹ½:____________
(4)ŌŚČÜŅŗIÖŠµĪČĖNaOHČÜŅŗ£¬æɹŪ²ģµ½µÄĻÖĻóŹĒ_______Ęä·“Ó¦µÄŌĄķŹĒ_________(Š“»Æѧ·½³ĢŹ½)”£
(5)¼ģŃéČÜŅŗJÖŠµÄ½šŹōŃōĄė×Ó£¬ÓĆ_______ŹŌ¼Į(Ģī»ÆѧŹ½)£¬ĘäĻÖĻóŹĒ__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”抓³öĻĀĮŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬²¢×¢Ć÷·“Ó¦ĄąŠĶ
£Ø1£©ÓɱūĻ©Öʱø¾Ū±ūĻ©µÄ·“Ó¦·“Ó¦ĄąŠĶ
£Ø2£©ÓĆ¼×±½ÖĘTNTµÄ·“Ó¦·“Ó¦ĄąŠĶ
£Ø3£©±½ÖĘäå±½·“Ó¦ĄąŠĶ
£Ø4£©ŅŅĻ©ĶØČėäåĖ®ÖŠ·“Ó¦ĄąŠĶ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com