
| A、2.0 | B、2.4 |
| C、2.5 | D、2.6 |
| 71g |
| 71g/mol |
| 71g |
| 67.5g/mol |
| 71×5 |
| 67.5 |
| 71 |
| 13.5 |
| 71 |
| 13.5 |
| 71 |
| 27 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | Ki=1.7×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、IBr是双原子分子 |
| B、在很多反应中,IBr是强氧化剂 |
| C、和NaOH溶液反应生成NaBr和NaIO |
| D、和水反应时,既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、质子数35、中子数45的原子:
| ||||||||
| B、HClO的结构式:H-Cl-O | ||||||||
C、过氧化钠的电子式:Na:
| ||||||||
D、硫离子的结构示意图: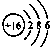 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、几千万年前地球上一条恐龙体内的某个原子可能在你的身体里 |
| B、在化学变化中,分子可以再分,离子和原子不可以再分 |
| C、一定条件下,金属钠可以成为绝缘体 |
| D、一定条件下,水在20℃时能凝固成固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com