某课外兴趣小组测定某品牌牛奶中钙的含量,方法如下:取100mL牛奶,加入足量的草酸铵[(NH
4)
2C
2O
4]溶液,使牛奶中的钙转化成难溶的CaC
2O
4沉淀;过滤,用适量的蒸馏水洗涤沉淀表面吸附的少量(NH
4)
2C
2O
4、蛋白质等杂质;将沉淀转移至锥形瓶中,加足量的稀硫酸溶液溶解CaC
2O
4;然后以0.10mol?L
-1的KMnO
4溶液滴定生成的H
2C
2O
4溶液,共消耗12.00mLKMnO
4溶液.发生的反应为:
5H
2C
2O
4+2KMnO
4+3H
2SO
4═5CO
2↑+2MnSO
4+K
2SO
4+8H
2O
(1)KMnO
4溶液应盛在
(填“酸式”或“碱式”)滴定管中.
(2)若滴定管的规格为25mL,滴定前滴定管中液面的读数为5.20mL,则滴定管中液体的体积为
(填代号).
A.5.20mL B.19.80mL C.大于19.80mL D.小于19.80mL
(3)本实验是否需要外加指示剂?
(填“是”或者“否”).到达滴定终点时,溶液的颜色由
色变为
色.
(4)滴定时边滴边摇动锥形瓶,眼睛应观察
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(5)该牛奶中钙的含量为
mg/100mL.
(6)下列操作会使实验结果偏低的是
(填代号)
A.滴定管未用KMnO
4溶液润洗就直接盛装KMnO
4溶液
B.向锥形瓶转移沉淀时,损失部分沉淀
C.开始时平视读数,滴定完成时俯视读数
D.CaC
2O
4的表面没有洗涤干净,吸附少量C
2O
42-等杂质
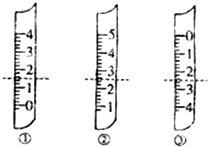
(7)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是
.
A.①是量简,读数为1.5mL
B.②是量筒,读数为2.5mL
C.③是滴定管,读数为2.50mL
D.②是温度计,读数是2.5℃





 新思维寒假作业系列答案
新思维寒假作业系列答案 某课外兴趣小组测定某品牌牛奶中钙的含量,方法如下:取100mL牛奶,加入足量的草酸铵[(NH4)2C2O4]溶液,使牛奶中的钙转化成难溶的CaC2O4沉淀;过滤,用适量的蒸馏水洗涤沉淀表面吸附的少量(NH4)2C2O4、蛋白质等杂质;将沉淀转移至锥形瓶中,加足量的稀硫酸溶液溶解CaC2O4;然后以0.10mol?L-1的KMnO4溶液滴定生成的H2C2O4溶液,共消耗12.00mLKMnO4溶液.发生的反应为:
某课外兴趣小组测定某品牌牛奶中钙的含量,方法如下:取100mL牛奶,加入足量的草酸铵[(NH4)2C2O4]溶液,使牛奶中的钙转化成难溶的CaC2O4沉淀;过滤,用适量的蒸馏水洗涤沉淀表面吸附的少量(NH4)2C2O4、蛋白质等杂质;将沉淀转移至锥形瓶中,加足量的稀硫酸溶液溶解CaC2O4;然后以0.10mol?L-1的KMnO4溶液滴定生成的H2C2O4溶液,共消耗12.00mLKMnO4溶液.发生的反应为: 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.