
温度为T ℃时,在体积为10 L的真空容器中通入1.00 mol氢气和1.00 mol碘蒸气,20 min后,反应达到平衡,此时测得碘蒸气的浓度为0.020 mol·L-1。涉及的反应可以用下面的两个化学方程式表示:
①H2(g)+I2(g)2HI(g)
②2H2(g)+2I2(g)4HI(g)
下列说法正确的是( )
A.反应速率用HI表示时,v(HI)=0.008 mol·L-1·min-1
B.两个化学方程式的意义相同,但其平衡常数表达式不同,不过计算所得数值相同
C.氢气在两个反应方程式中的转化率不同
D.第二个反应中,增大压强平衡向生成HI的方向移动
科目:高中化学 来源: 题型:
硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)硅在元素周期表中的位置是________。
(2)工业上生产粗硅的反应有:SiO2+2C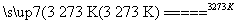 Si(粗)+2CO↑;SiO2+3C
Si(粗)+2CO↑;SiO2+3C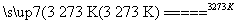 SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1∶1,则参加反应的C和SiO2的物质的量之比为________。
SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1∶1,则参加反应的C和SiO2的物质的量之比为________。
(3)工业上可以通过如图所示的流程制取纯硅:
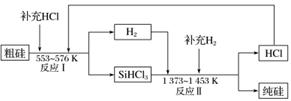
①若反应Ⅰ为Si(粗)+3HCl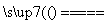 SiHCl3+H2,则反应Ⅱ的化学方程式为________________________。
SiHCl3+H2,则反应Ⅱ的化学方程式为________________________。
②整个制备过程中必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式:__________________。
③假设每一轮次制备1 mol纯硅,且生产过程中硅元素没有损失,反应Ⅰ中HCl的利用率为90%,反应Ⅱ中H2的
利用率为93.75%,则在第二轮次的生产中,补充投入HCl和H2的物质的量之比是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
①氯气的性质活泼,它与氢气混合后立即发生爆炸 ②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收 ③新制氯水的氧化性强于久置氯水的 ④检验HCl气体中是否混有Cl2,方法是将气体通入硝酸银溶液 ⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水中
A.①②③ B.②③④ C.③ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(NH4)2CO3(s)===NH4HCO3(s)+NH3(g) ΔH=74.9 kJ·mol-1。下列说法中正确的是( )
A.该反应中熵变小于0,焓变大于0
B.该反应是吸热反应,因此一定不能自发进行
C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行
D.判断反应能否自发进行需要根据ΔH与ΔS综合考虑
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)CO(g)+H2(g)。不能确定上述可逆反应在一定条件下已达到化学平衡状态的是( )
A.体系的体积不再发生变化
B.v正(CO)=v逆(H2O)
C.生成n mol CO的同时生成n mol H2
D.1 mol H—H键断裂的同时断裂2 mol H—O键
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)2NO2(g),随温度升高,混合气体的颜色变深。

回答下列问题:
(1)反应的ΔH______0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s时段,反应速率v(N2O4)为__________________ mol·L-1·s-1;反应的平衡常数K1为________________。
(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4)以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
①T________100 ℃(填“大于”或“小于”),判断理由是
________________________________________________________________________
________________________________________________________________________。
②列式计算温度T时反应的平衡常数K2________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①1/4CaSO4(s)+CO(g)1/4CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1
②CaSO4(s)+CO(g)CaO(s)+CO2(g)+SO2(g) ΔH2=+210.5 kJ·mol-1
③CO(g)1/2C(s)+1/2CO2(g)
ΔH3=-86.2 kJ·mol-1
(1)反应2CaSO4(s)+7CO(g)CaS(s)+CaO(s)+6CO2(g)+C(s)+SO2(g)的ΔH=____________(用ΔH1、ΔH2和ΔH3表示)。
(2)反应①~③的平衡常数的对数lgK随反应温度T的变化曲线如图所示,结合各反应的ΔH,归纳lgKT曲线变化规律:
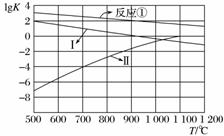
a)________________________________________________________________________;
b)________________________________________________________________________。
(3)向盛有CaSO4的真空恒容密闭容器中充入CO,反应①于900 ℃达到平衡,c平衡(CO)=8.0×10-5 mol·L-1,计算CO的转化率(忽略副反应,结果保留两位有效数字)。
(4)为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入________。
(5)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生CaSO4,该反应的化学方程式为________________________;在一定条件下,CO2可与对二甲苯反应,在其苯环上引入一个羧基,产物的结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CO(g)+H2O(g)CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
请回答下列问题:
(1)上述反应的化学平衡常数表达式为____________。该反应的Q______0(填“>”或“<”)。
(2)850 ℃时在体积为10 L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的物质的量浓度变化如图所示,则0~4 min时平均反应速率v(CO)=____________。
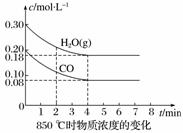
(3)若在500 ℃时进行。且CO、H2O(g)的起始浓度均为0.020 mol·L-1 ,该条件下,CO的最大转化率为 。
(4)若在850 ℃时进行,设起始时CO和H2O(g)共为1 mol,其中H2O(g)的体积分数为x,平衡时CO的转化率为y,试推导y随x变化的函数关系式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com