
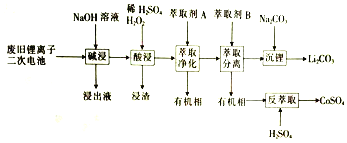
【题目】从废旧锂离子二次电池(主要成分为![]() ,还含有少量石墨和金属钢売、铝箔等杂质)中回收钴和锂的工艺流程如下:回答下列问题:
,还含有少量石墨和金属钢売、铝箔等杂质)中回收钴和锂的工艺流程如下:回答下列问题:
(1)![]() 的电子式为__________。“碱浸”的目的是____________。
的电子式为__________。“碱浸”的目的是____________。
(2)“酸浸”过程中![]() 发生反应的离子方程式为______________,浸渣中含有的主要成分是_______________________。
发生反应的离子方程式为______________,浸渣中含有的主要成分是_______________________。
(3)“萃取净化”除去的杂质离子除![]() 外,还有________(填离子符号)
外,还有________(填离子符号)
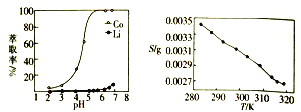
(4)“苯取分离“中钴、锂的萃取率与平衡时溶液![]() 的关系如图所示,
的关系如图所示,![]() 一般选择5左右,理由是_____________________________________。
一般选择5左右,理由是_____________________________________。
(5)“沉锂“中![]() 的溶解度随温度变化的曲线如图所示:
的溶解度随温度变化的曲线如图所示:
①根据平衡原理分析![]() 在水中的溶解度随温度变化的原因______________。
在水中的溶解度随温度变化的原因______________。
②为获得高纯![]() ,提纯操作依次为热过滤、_______、烘干。
,提纯操作依次为热过滤、_______、烘干。
③若“沉锂”中![]() ,加入等体积等浓度
,加入等体积等浓度![]() 溶液,则此时沉锂率为________________。(已知
溶液,则此时沉锂率为________________。(已知![]() 的
的![]() 为
为![]() )
)
【答案】![]() 除去铝
除去铝 ![]() 石墨
石墨 ![]()
![]() 在5左右时钴、锂的分离效率最高
在5左右时钴、锂的分离效率最高 ![]() 溶解过程为放热反应,温度升高,溶解度减少 洗涤 88.0%
溶解过程为放热反应,温度升高,溶解度减少 洗涤 88.0%
【解析】
废旧锂离子二次电池含有LiCoO2、少量石墨和镀镍金属钢壳、铝箔以及钙,加入氢氧化钠溶液除去铝。碱浸后的固体中加入硫酸和双氧水与LiCoO2反应生成Li2SO4和COSO4,硫酸与金属钢壳反应,会有少量二价亚铁离子的生成,在双氧水的作用下,转化为三价铁离子,分离出浸渣。滤液中加入萃取剂A,除去Ni2+、Fe3+。“萃取净化”后的溶液中加入萃取剂B,“苯取分离“钴和锂,有机相中加入硫酸反萃取,生成CoSO4,水溶液中加入Na2CO3生成Li2CO3沉淀,据此分析解答。
(1)![]() 为离子化合物,电子式为
为离子化合物,电子式为![]() ;废旧锂离子二次电池含有LiCoO2、少量石墨和镀镍金属钢壳、铝箔等,加入氢氧化钠溶液,只有铝与其反应,其他成分不反应,故目的是除去铝。
;废旧锂离子二次电池含有LiCoO2、少量石墨和镀镍金属钢壳、铝箔等,加入氢氧化钠溶液,只有铝与其反应,其他成分不反应,故目的是除去铝。
因此,本题正确答案是:![]() ;除去铝;
;除去铝;
(2)LiCoO2中钴显+3价,从后面可以看出钴显+2价,除加入硫酸和双氧水外,没有加入还原剂了,所以双氧水作还原剂,生成氧气,故离子方程式为![]() ;石墨不溶解,存在于滤渣中。
;石墨不溶解,存在于滤渣中。
因此,本题正确答案是:![]() ;石墨;
;石墨;
(3)二次电池中含有镀镍金属钢壳,加入硫酸,会有少量二价亚铁离子的生成,在双氧水的作用下,转化为三价铁离子,存在于滤液中,故加入萃取液A,净化时,除了镍离子外,还有少量的铁离子。
因此,本题正确答案是:![]() ;
;
(4)由图可知,pH值2~5,随pH值的增加,萃取率在增加,当pH达到5左右,萃取率很高,接近100%,而若pH值再增加,萃取锂的含量将增加,萃取钴纯度下降,故pH一般选择5左右进行萃取实验,使分离效率最高。
因此,本题正确答案是:![]() 在5左右时钴、锂的分离效率最高;
在5左右时钴、锂的分离效率最高;
(5)①由图可知,溶解度随温度的升高而降低,根据平衡移动的原理,温度升高,平衡向吸热方向进行,故此溶解为放热过程。
因此,本题正确答案是:![]() 溶解过程为放热反应,温度升高,溶解度减少;
溶解过程为放热反应,温度升高,溶解度减少;
② 对物质进行提纯,在过滤和烘干之间,必须洗涤,以保证得到物质纯度较高。
因此,本题正确答案是:洗涤;
③加入等体积等浓度Na2CO3溶液,加入后体积变为原来的两倍,故浓度变为原来的一半,即c(Li+)=c(CO32-)=0.5mol/L,2Li++CO32-=Li2CO3,故碳酸根过量,反应后c(CO32-)=0.25mol/L,根据![]() 为
为![]() ,从而求得c(Li+)=0.06mol/L,故沉锂率为
,从而求得c(Li+)=0.06mol/L,故沉锂率为![]() 100%=88.0%。
100%=88.0%。
因此,本题正确答案是:88.0%。


科目:高中化学 来源: 题型:
【题目】硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法错误的是

A. 碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂
B. 为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C. 可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D. 常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废蚀刻液(含![]() 及
及![]() )制备碱性蚀刻液[
)制备碱性蚀刻液[![]() 溶液]和
溶液]和![]() 的主要步骤:用
的主要步骤:用![]() 氧化废蚀刻刻液,制备氨气,制备碱性蚀刻液[
氧化废蚀刻刻液,制备氨气,制备碱性蚀刻液[![]() ],固液分离,用盐酸溶解沉淀并制备
],固液分离,用盐酸溶解沉淀并制备![]() ,下列实验装置和操作不能达到实验目的的是
,下列实验装置和操作不能达到实验目的的是
A.  制备
制备![]()
B. 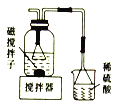 制备
制备![]() 并得到
并得到![]()
C. 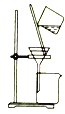 分离
分离![]() 溶液和
溶液和![]()
D. 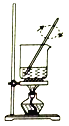 将
将![]() 溶液蒸干制备
溶液蒸干制备![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿水青山就是金山银山”,研究NO2、NO、CO、NO2等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)已知:①NO2(g) + CO(g)![]() CO2(g) + NO(g)ΔH=-234 kJ/mol该反应的平衡常数为K1(下同)
CO2(g) + NO(g)ΔH=-234 kJ/mol该反应的平衡常数为K1(下同)
②N2(g)+O2(g) ![]() 2NO(g) ΔH=+179.5 kJ/mol K2
2NO(g) ΔH=+179.5 kJ/mol K2
③2NO(g) +O2(g)![]() 2NO2(g) ΔH=-112.3 kJ/mol K3
2NO2(g) ΔH=-112.3 kJ/mol K3
试写出NO与CO反应生成无污染物气体的热化学方程式____________________;
以及此热化学方程式的平衡常数K=________(用K1、K2、K3表示)。
(2)①一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图1所示。温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是________。

②已知:测定空气中NO和CO含量常用的方法有两种:
方法1:电化学气敏传感器法。其中CO传感器的工作原理如图2所示,则工作电极的反应式为____;
方法2:氧化还原滴定法。用H2O2溶液吸收尾气、将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度。写出NO与H2O2溶液反应的离子方程式:________________。
(3)NO2会污染环境,可用Na2CO3溶液吸收NO2 并生成CO2,已知9.2gNO2气体和Na2CO3溶液完全反应时转移电子0.1mol,恰好反应后,使得溶液中的CO2完全逸出,所得溶被呈弱碱性,则溶液中存在的所有离子浓度大小关系是____________________________。
(4)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图I、Ⅱ所示。

①由图I知,当废气中的NO含量增加时,宜选用___________法提高脱氮的效率。
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+,提高了脱氮的效率,其可能原因为___________。
(5)研究表明:NaClO/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。温度高于60℃后,NO去除率下降的原因为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院大连化学物理研究所的“甲醇制取低碳烯经(![]() 技术”获得国家科学技术发明一等奖,该技术先由煤气化制合成气再由合成气制甲醇和氨气,最后由甲醇制乙烯和丙烯。
技术”获得国家科学技术发明一等奖,该技术先由煤气化制合成气再由合成气制甲醇和氨气,最后由甲醇制乙烯和丙烯。
(1)煤气化包含一系列化学反应,已知热化学方程式:
![]()
![]()
![]()
![]()
则反应![]()
![]() _____
_____![]()
(2)以投料比![]() 合成甲醇:
合成甲醇:![]() ,温度、压强与
,温度、压强与![]() 的平衡转化率的关系如图所示
的平衡转化率的关系如图所示
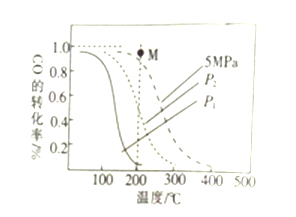
回答下列问题:
①![]() _____(填>”或“<)0
_____(填>”或“<)0
②![]() ______(填“>“或“<”)
______(填“>“或“<”)![]()
③![]() ,
,![]() 时,
时,![]() 点的
点的![]() _____(填>”或"<")
_____(填>”或"<")![]() 。
。
④若起始时提高投料比![]() 的平衡转化率将_______(填”増大”或“减小”)。
的平衡转化率将_______(填”増大”或“减小”)。
⑤参照下表,实际工业生产中大多采用![]() 和
和![]() ,其优点是____________。
,其优点是____________。
span>方法 | 催化剂 | 条件 | 备注 | 特点 | |
压力 | 温度 | ||||
高压法 |
二元催化剂 | 25~30 | 380~400 | 1924年工业化 | (1)催化剂不易中毒,再生困难 (2)副反应多 |
低压法 |
三元催化剂 | 5 | 230~270 | 1966年工业化 | (1)催化剂易中毒,再生容易,寿命为1~2年 (2)副反应少 |
(3)![]() 和
和![]() 生成
生成![]() 的反应为
的反应为![]()
![]() ,在
,在![]() 催化剂作用下的反应历程如下(
催化剂作用下的反应历程如下(![]() 表示吸附态)
表示吸附态)
化学吸附:![]() ;
;![]()
表面反应![]() ;
;![]() ,
,![]()
脱附:![]()
其中,![]() 的吸附分解反应活化能高,速率慢,决定了合成氨的整体反应速率.
的吸附分解反应活化能高,速率慢,决定了合成氨的整体反应速率.
①有利于提高合成氨平衡产率的条件有______(填字母)
A 低温 B 高温 C 低压 D 高压 E 催化剂
②标准平衡常数![]() =
=![]() ,其中
,其中![]() 为标准压强(
为标准压强(![]() ),
),![]() 、
、![]() 和
和![]() 为各组分的平衡分压,如
为各组分的平衡分压,如![]() ,
,![]() 为平衡总压,
为平衡总压,![]() 为平衡系统中
为平衡系统中![]() 的物质的量分数.已知起始时向一密闭容器中投入
的物质的量分数.已知起始时向一密闭容器中投入![]()
![]() 和
和![]()
![]() ,反应
,反应![]()
![]() +
+![]()
![]()
![]()
![]() 在恒定温度和标准压强下进行,
在恒定温度和标准压强下进行,![]() 的平衡产率为
的平衡产率为![]() ,则该反应的
,则该反应的![]() =________(用含
=________(用含![]() 的代数式表示)。下图中可以表示标准平衡常数随温度
的代数式表示)。下图中可以表示标准平衡常数随温度![]() 的变化趋势的是____________(填字母)
的变化趋势的是____________(填字母)
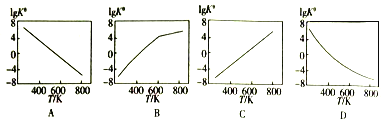
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早在2000多年前,人们发现柳树皮中含有一种具有解热镇痛功效的物质—水杨酸,此后科学家对水杨酸的结构进行一系列改造,合成出疗效更佳的长效缓释阿司匹林,其开发过程蕴含着重要的思想方法,请回答下列问题:
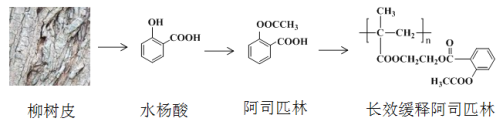
(1)水杨酸的结构与性质
①水杨酸中含氧官能团的名称是____________、______________。
②下列关于水杨酸的说法正确的是__________。
A.分子式为C7H7O3
B.1 mol水杨酸能与2 molNaOH反应
C.可发生加成、取代、消去反应
(2)水杨酸的合成

①由![]() 制
制![]() ,不采取甲苯直接与Br2直接反应,而是经过步骤①~③,目的是_______________
,不采取甲苯直接与Br2直接反应,而是经过步骤①~③,目的是_______________
②步骤④~⑥的顺序能够改为水解、酸化、氧化?____________(填“能”或“不能”),理由是__________________________________
(3)水杨酸具有解热镇痛的功效,但是其酸性很强,对人的肠胃有刺激性,容易引发胃溃疡,1897年德国化学家菲利克斯·霍夫曼对水杨酸的结构进行改造合成出阿司匹林。
①水杨酸的酸性主要来源于-COOH,将-OH转化为-OOCCH3,可使-COOH的酸性大大降低。科学家的这一设计思路依据的原理是_________________________________________
②水杨酸到阿司匹林的反应类型是_________
(4)1982年拜尔公司将阿司匹林与聚甲基丙烯酸借助乙二醇嫁接起来,研制出长效缓释阿司匹林,可减少每天吃药次数,大大方便了人们对药物的使用。
①长效缓释阿司匹林在人体内释放出阿司匹林的反应类型是______________
②写出乙烯经2步合成乙二醇的化学方程式_______________________、________________
③以烃A为原料,合成聚甲基丙烯酸的路线如下:

已知:

(R、R’为烃基或氢原子)
请填写有机物A~D的结构简式,在所有箭头上标注试剂和条件_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列物质在水溶液中的电离方程式:
(1)HClO___________________________________________________
(2)Ba(NO3)2______________________________________________
A层:(3)NaHSO4____________________________________________
NH3·H2O_____________________________________________________
B层:(3)H2CO3______________________________________________
Fe(OH)3____________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物环丁基甲酸(H)是一种应用广泛的有机物,合成化合物H的路线如图:

(1)A属于烯烃,其结构简式为______________,由A→B的反应类型是___________。
(2)D中官能团的名称是_________________,由D→E的反应类型是________________。
(3)E的名称是_______________。
(4)写出F与NaOH溶液反应的化学方程式_______________________。
(5)M是G的同分异构体,且满足以下条件:①能使溴的四氯化碳溶液褪色;②1mol M与足量饱和NaHCO3反应产生88g气体;③核磁共振氢谱为2组峰;则M的结构简式为(不考虑立体异构,只写一种)________________,N是比M少一个碳原子的同系物,则N的同分异构体有_________种。
(6)参照上述合成路线,以![]() 和化合物E为原料(无机试剂任选),设计制备
和化合物E为原料(无机试剂任选),设计制备![]() 的合成路线________________________________。
的合成路线________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲,可能含NO、CO2、NO2、N2中的几种,将一定量的甲气体经过如图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )
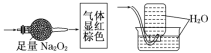
A.NO2、N2B.NO、CO2
C.NO2、CO2D.NO、CO2、N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com