

| A. | 锌片发生的变化均为:Zn-2e-=Zn2+ | |
| B. | 化学能转化为电能的转换率(η):η丙>η乙>η甲 | |
| C. | 一段时间后的电解质溶液的温度(T):T甲<T乙<T丙 | |
| D. | 甲、乙、丙的总反应均为:Zn+Cu2+=Zn2++Cu |
分析 A.锌活泼性大于铜,可以和铜盐溶液发生置换反应,甲为化学腐蚀,乙和丙为电化腐蚀,锌做负极失电子发生氧化反应;
B.化学能转化为电能转化率,丙装置中盐桥避免了离子碱的作用,甲装置开始不能形成原电池,析出铜在锌表面时形成原电池反应;
C.反应过程中丙装置中离子间干扰少溶液温度低;
D.反应实质都是锌和硫酸铜溶液的反应.
解答 解:A.锌活泼性大于铜,可以和铜盐溶液发生置换反应,甲为化学腐蚀,乙和丙为电化腐蚀,锌做负极失电子发生氧化反应,锌片发生的变化均为:Zn-2e-=Zn2+,故A正确;
B.化学能转化为电能转化率,丙装置中盐桥避免了离子碱的作用,甲装置开始不能形成原电池,析出铜在锌表面时形成原电池反应,乙形成原电池反应,化学能转化为电能的转换率(η):η丙>η乙>η甲,故B正确;
C.反应过程中丙装置中离子间干扰少溶液温度低,甲中反应过程中离子间影响大,温度高,故C错误;
D.反应实质都是锌和硫酸铜溶液的反应,甲、乙、丙的总反应均为:Zn+Cu2+=Zn2++Cu,故D正确;
故选C.
点评 本题考查了原电池原理、电极名称、电极反应、电能的转换率等,注意盐桥的作用,掌握基础是解题关键,题目难度中等.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氚表示为 ${\;}_{1}^{3}$T | B. | NaClO的电子式 | ||
| C. | “生石膏”的化学式CaSO4•2H2O | D. | 氯离子的结构示意图  |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,0.1mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者中所占物质的量分数(分布系数)随pH变化的关系如图所示.下列表述不正确的是( )
常温下,0.1mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者中所占物质的量分数(分布系数)随pH变化的关系如图所示.下列表述不正确的是( )| A. | HC2O4-?H++C2O42- K=1×10-4.3 | |
| B. | 在 0.1 mol/LNaHC2O4溶液中,各离子浓度大小关系为:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-) | |
| C. | 常温下HF的 Ka=1×10-3.45,将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F-═HF+HC2O4- | |
| D. | 将等物质的量的NaHC2O4、Na2C2O4溶于水中,所得溶液pH恰好为4.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光照}{→}$CH2Cl2+H2 | |
| B. |  +HO-NO2$→_{△}^{浓硫酸}$ +HO-NO2$→_{△}^{浓硫酸}$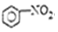 +H2O +H2O | |
| C. | H2C=CH2+Br2→CH3CHBr2 | |
| D. | CH3CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com