
Ņ»¶ØĪĀ¶ČĻĀ£¬ĻņĢå»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ³äČė1mol PCl5(g)£¬·¢Éś·“Ó¦£ŗ
PCl5(g)  PCl3(g) +Cl2(g) ”÷H=+Qkj.mol-1 Ī¬³ÖČŻĘ÷ĪĀ¶Č²»±ä£¬²āµĆČŻĘ÷ÄŚŃ¹ĒæĖę·“Ó¦Ź±¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
PCl3(g) +Cl2(g) ”÷H=+Qkj.mol-1 Ī¬³ÖČŻĘ÷ĪĀ¶Č²»±ä£¬²āµĆČŻĘ÷ÄŚŃ¹ĒæĖę·“Ó¦Ź±¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. 3sÄŚµÄĘ½¾łĖŁĀŹĪŖ£ŗv(PCl3)=0.1 mol”¤L-1.s-1
B£®“ļµ½Ę½ŗāŹ±·Å³ö0.6Q kJČČĮæ
C£®ĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬Ę½ŗā³£Źż¼õŠ”
D£®ĘäĖūĢõ¼ž²»±ä£¬ŌŁĻņČŻĘ÷ÖŠ³äČė1mol PCl5(g)£¬Ōņ“ļŠĀĘ½ŗāŹ±£¬c(PCl5)>0.4mol”¤L-1
AD
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗAĻīŗćĪĀ”¢ŗćČŻµÄĆܱÕČŻĘ÷ÖŠ£¬ĘųĢåµÄĪļÖŹµÄĮæÖ®±ČµČÓŚŃ¹ĒæÖ®±Č£¬ŌņĘ½ŗāŹ±»ģŗĻĘųĢåµÄĪļÖŹµÄĮæĪŖ1.6mol£¬ĘųĢåµÄĪļÖŹµÄĮæŌö“ó£Ø1.6-1£©mol=0.6mol£¬ÉčÉś³ÉPCl3µÄĪļÖŹµÄĮæĪŖx£¬
PCl5£Øg£©?PCl3£Øg£©+Cl2£Øg£© ĘųĢåŌö¼ÓµÄĪļÖŹµÄĮæ
1mol 1mol
x 0.6mol
½āµĆx=0.6mol£¬V£ØPCl3£©£½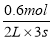 £½0.1mol/£ØL£®s£©£¬ÕżČ·£»
£½0.1mol/£ØL£®s£©£¬ÕżČ·£»
BĻīøĆ·“Ó¦ŹĒĪüČČ·“Ó¦²»ŹĒ·ÅČČ·“Ó¦£¬µ±ĘųĢåŌö¼Ó1molŹ±ĪüŹÕµÄČČĮæŹĒQKJ£¬ŌņĘųĢåŌö¼Ó0.6molŹ±ĪüŹÕµÄČČĮæŹĒ0.6QKJ£¬“ķĪó£»CĻīĪĀ¶Č²»±ä£¬Ę½ŗā³£Źż²»±ä£¬“ķĪó£»DĻīĘ½ŗāĢåĻµÖŠŌŁ¼ÓČė1molµÄPCl5£¬ÖŲŠĀµ½“ļĘ½ŗāדĢ¬£¬æÉŅŌµČŠ§ĪŖæŖŹ¼¼ÓČė2molµÄPCl5£¬Ģå»żŌö“óĪŖŌĄ“µÄ2±¶£¬“ļĘ½ŗā£ØøĆĘ½ŗāÓėŌĘ½ŗāµČŠ§£©ŗóŌŁ½«Ģå»żŃ¹Ėõµ½ŌĄ““󊔣¬ÓėŌĘ½ŗāĻą±Č£¬Ń¹ĒæŌö“ó£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ŌņĘ½ŗāÅØ¶Č“óÓŚŌĄ“µÄĮ½±¶£¬¼“c(PCl5)>0.4mol”¤L-1£¬ÕżČ·”£
æ¼µć£ŗæ¼²é»Æѧ·“Ó¦ĖŁĀŹŗĶ»ÆŃ§Ę½ŗā”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”ÄĻ¾©ŹŠøßŅ»ĻĀѧʌʌĩѧĒéµ÷ŃŠ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø10·Ö£©ŠÅĻ¢Ź±“ś²śÉśµÄ“óĮæµē×ÓĄ¬»ų¶Ō»·¾³¹¹³ÉŃĻÖŲĶžŠ²”£Ä³ŃŠ¾æŠŌѧĻ°Š”×齫Ņ»Åś·ĻĘśµÄĻßĀ·°å¼ņµ„“¦Ąķŗó£¬µĆµ½ŗ¬Cu”¢Fe¼°ÉŁĮæAu”¢PtµČ½šŹōµÄ»ģŗĻĪļ£¬²¢ÓĆČēĻĀĮ÷³ĢÖʱøµØ·Æ¾§Ģå£ØCuSO4?5H2O£©£ŗ

ŅŃÖŖ£ŗ²æ·ÖŃōĄė×ÓŅŌĒāŃõ»ÆĪļŠĪŹ½³ĮµķŹ±ČÜŅŗµÄpH¼ūĻĀ±ķ£ŗ
ŃōĄė×Ó | Fe3+ | Fe2+ | Cu2+ |
æŖŹ¼³Įµķ | 1.5 | 6.4 | 4.2 |
ĶźČ«³Įµķ | 3.2 | 8.9 | 6.7 |
£Ø1£©ĀĖŌü¢ńµÄÖ÷ŅŖ³É·ŻŹĒ£ØŠ“»ÆѧŹ½£©______”£
£Ø2£©·“Ó¦¢ņÖŠ¼ÓČėH2O2µÄ×÷ÓĆŹĒ______”£
£Ø3£©³Įµķ¹ż³ĢÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ÓŠ______”¢______”£
£Ø4£©²Ł×÷¢ńµÄ²½ÖčŹĒ______”¢______”¢¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”£
£Ø5£©²ā¶ØµØ·Æ¾§Ģå“æ¶ČµÄŹµŃé²½ÖčČēĻĀ£ŗ
a. ×¼Č·³ĘČ”3.125gµØ·Æ¾§ĢåѳʷÅä³É100mLČÜŅŗ£»
b. Č”10.00 mLČÜŅŗÓŚ“ųČū׶ŠĪĘæÖŠ£¬¼ÓŹŹĮæĖ®Ļ”ŹĶ£¬¼ÓČė¹żĮæKI¹ĢĢ壬·¢Éś·“Ó¦£ŗ
2Cu2+ +4I”„= 2CuI”ż + I2
c. ¼ĢŠųĻņÉĻŹö»ģŗĻĪļÖŠ£¬ÖšµĪ¼ÓČė0.1000 mol”¤L-1Na2S2O3ČÜŅŗÖĮĒ”ŗĆĶźČ«·“Ó¦£¬¹²ĻūŗÄ12. 00mL Na2S2O3ČÜŅŗ£ŗI2£«2S2O = 2I”„£«S4O
= 2I”„£«S4O
Ēóѳʷ֊µØ·Æ¾§ĢåµÄÖŹĮæ·ÖŹż£ØŠ“³ö¼ĘĖć¹ż³Ģ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”ÄĻ¾©ŹŠÓź»ØĒųøßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ¹ż³Ģ·¢ÉśĮĖ»Æѧ·“Ó¦µÄŹĒ
A£®ÓĆ×ŌĄ“Ė®ÖĘÕōĮóĖ® B£®“Óŗ£Ė®ÖŠ»ńµĆĀČ»ÆÄĘ
C£®ĆŗµÄøÉĮó D£®ŹÆÓĶµÄ·ÖĮó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕŹ”ÄĻ¾©ŹŠÓź»ØĒųøßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
·ÅÉäŠŌĶ¬Ī»ĖŲÓĖ µÄŌ×ÓŗĖÄŚµÄÖŠ×ÓŹżŹĒ
µÄŌ×ÓŗĖÄŚµÄÖŠ×ÓŹżŹĒ
A£®51 B£®92 C£®143 D£®235
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕĖŽĒØŹŠøßŅ»ĻĀѧʌʌĩ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
SF6ŹĒŅ»ÖÖÓÅĮ¼µÄ¾ųŌµĘųĢ壬·Ö×Ó½į¹¹ÖŠÖ»“ęŌŚS-F¼ü”£ŅŃÖŖ£ŗ 1molS(s)×Ŗ»ÆĪŖĘųĢ¬ĮņŌ×ÓĪüŹÕÄÜĮæ280kJ,¶ĻĮŃ1molF-F ”¢S-F¼üŠčĪüŹÕµÄÄÜĮæ·Ö±šĪŖ160kJ”¢330kJ”£ŌņS(s)£«3F2(g)=SF6(g)µÄ·“Ó¦ČČ”÷HĪŖ
A£®-1780kJ/mol B£®+1220 kJ/mol C£®-1220 kJ/mol D£®+1780 kJ/mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕĖŽĒØŹŠøßŅ»ĻĀѧʌʌĩ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
T”ꏱ£¬ŌŚ1 LµÄĆܱÕČŻĘ÷ÖŠ³äČė2 mol CO2ŗĶ6mol H2£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗ
CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ”÷H=£49.0kJ/mol
CH3OH(g)+H2O(g) ”÷H=£49.0kJ/mol
²āµĆH2ŗĶCH3OH(g)µÄÅضČĖꏱ¼ä±ä»ÆČēÓŅĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©

A£®0~10minÄŚv(H2)=0.3mol/(L”¤min)
B£®T”ꏱ£¬Ę½ŗā³£Źż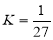 £¬CO2ŗĶH2µÄ×Ŗ»ÆĀŹĻąµČ
£¬CO2ŗĶH2µÄ×Ŗ»ÆĀŹĻąµČ
C£®T”ꏱ£¬ÉĻŹö·“Ó¦ÖŠÓŠ64g CH3OHÉś³É£¬Ķ¬Ź±·Å³ö98.0kJµÄČČĮæ
D£®“ļµ½Ę½ŗāŗó£¬ÉżøßĪĀ¶Č»ņŌŁ³äČėCO2ĘųĢ壬¶¼æÉŅŌĢįøßH2µÄ×Ŗ»ÆĀŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014½ĖÕĖŽĒØŹŠøßŅ»ĻĀѧʌʌĩ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŌĻĀŹµŃé²Ł×÷ÕżČ·µÄŹĒ( )
A£®ÓĆĮæĶ²ĮæČ”5.0mLÅØĮņĖį²¢Ö±½ÓŌŚĮæĶ²ÖŠĻ”ŹĶ
B£®³ĘĮæNaOH¹ĢĢåŹ±£¬½«Ņ©Ę·Ö±½Ó·ÅŌŚĶŠÅĢÉĻ
C£®øųÉÕĘæĄļµÄŅŗĢå¼ÓČČŹ±£¬µęÉĻŹÆĆŽĶų
D£®ÓĆ×ģ“µĆšČ¼×ÅµÄ¾Ę¾«µĘ»šŃę
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ćĪ÷¹šĮÖŹŠĻĀѧʌø߶žÄź¼¶ĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø6·Ö£©°“ĻĀĶ¼×°ÖĆ½ųŠŠŹµŃ飬»Ų“šĻĀĮŠĪŹĢā£ØC”¢C1”¢C2¾łĪŖŹÆÄ«µē¼«£©”£

£Ø1£©Ģśµē¼«ĪŖ__________¼«£¬µē¼«·“Ó¦Ź½ĪŖ__________£»
£Ø2£©ŹÆÄ«°ōC1ĪŖ__________¼«£¬ŹÆÄ«°ōC2ø½½üµÄŹµŃéĻÖĻóĪŖ____________________”£
£Ø3£©µ±C2¼«²śÉś2£®24 LĘųĢå£Ø±ź×¼×“Ģ¬£©Ź±£¬AÖŠCuSO4ČÜŅŗµÄÖŹĮæøıäĮĖ__________g”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ć¶«ÕŲĒģŹŠ±ĻŅµ°ąµŚ¶ž“ĪÄ£Äāæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ( )
A£®¹żŃõ»ÆÄĘŗĶĖ®·“Ó¦£ŗ2Na2O2+2H2O=4Na++4 OH”Ŗ+O2”ü
B£®ÓĆĶĪŖµē¼«µē½ā±„ŗĶŹ³ŃĪĖ®£ŗ2Cl”Ŗ+2H2OĶصēCl2”ü+H2”ü+2OH”Ŗ
C£®ŌŚĆ÷·ÆČÜŅŗÖŠµĪ¼Ó¹żĮæ°±Ė®£ŗAl3++3NH3”¤H2O=Al(OH)3”ż+3NH4+
D£®ĻņŠ”ĖÕ“ņČÜŅŗÖŠ¼ÓÉŁĮæBa(OH)2ČÜŅŗ£ŗHCO3£+Ba2++OH£=BaCO3”ż+H2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com