
【题目】下列说法正确的是( )
A.苯酚与乙醇的官能团都是羟基
B.炔烃的官能团是碳碳双键
C.官能团是反映一类化合物物理性质的原子或原子团
D.饱和一元羧酸的通式为CnH2n+2O2
科目:高中化学 来源: 题型:
【题目】人们对苯及芳香烃的认识是一个不断深化的过程。
(1)已知分子式为C6H6的烃结构有多种,其中的两种为![]()
①下列反应中Ⅰ能________(填字母)而Ⅱ不能。
a.被酸性高锰酸钾溶液氧化 b.与溴水发生加成反应
c.与液溴发生取代反应 d.在空气中可以燃烧
②1 mol 物质与H2加成时, Ⅰ 需H2________mol,而 Ⅱ 需H2________mol。
③Ⅰ的一氯取代产物有_______种,Ⅱ的二氯取代产物有______种
![]()
(2)今发现C6H6还可能有另一种立体结构(如图所示),该结构的二氯代物有____________种。
(3)下列四种芳香烃中,属于苯的同系物的是______
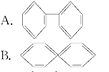
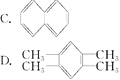
(4)现代化学认为苯分子中碳碳之间的键是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1molX气体和amolY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g) ![]() 2Z(g)反应一段时间后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a的值为( )
2Z(g)反应一段时间后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a的值为( )
A. 4B. 3C. 2D. 1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组采用下列装置,对浓硝酸与木炭的反应进行探究:
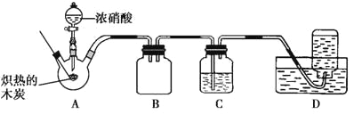
请回答下列问题:
(1)检验装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,伸入三颈烧瓶中,并塞紧瓶塞, 滴加浓硝酸。可以观察到三颈烧瓶中气体的颜色为______,产生该气体的化学方程式是______。
(2)装置 C 中盛有足量的浓 Ba(OH)2 溶液,反应一段时间后可观察到 C 中出现白色沉淀,该白色沉淀为__(写化学式)。
(3)装置 B 的作用是______。
(4)装置 D 中收集到了无色气体,部分同学认为是 NO,但有同学认为是 O2。下列对该气体的检验方法合适的是_____(填字母代号)。
A.敞口观察装置 D 中集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察石蕊试纸是否变红
C.带火星的木条伸入集气瓶内,观察木条是否复燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如下图所示
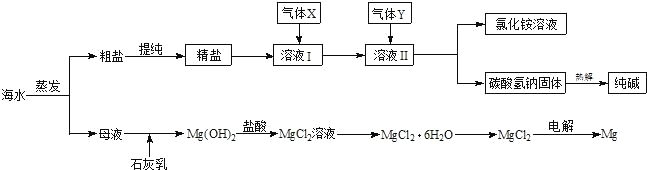
(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解;②加过量的 BaCl2 溶液;③加过量的 NaOH 溶液;④加过量的 Na2CO3 溶液;⑤______;⑥加适量的盐酸;⑦蒸发结晶。
(2)碳酸氢钠固体受热分解的化学方程式是:_____。
(3)Mg(OH)2 沉淀中因混有 Ca(OH)2,可选用______溶液进行洗涤以除之。
(4)高温灼烧六水合氯化镁晶体(MgCl2·6H2O)所得固体是氧化镁,试写出该反应的化学方程式:______。
(5)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,常用Fe2(SO4)3溶液作腐蚀液,腐蚀铜质电路板得到废液主要成分是FeSO4和CuSO4,含少量Fe2(SO4)3。某小组设计装置从废液中提取铜,如图:

已知:Fe2+失电子能力比OH-强。下列说法正确的是
A. 电解初期阴极没有铜析出,原因是2H+ + 2e- = H2↑
B. 石墨极的电极反应式为2H2O + 4e- = 4H+ + O2↑
C. 若将废液2充入阳极室时可再生腐蚀液(硫酸铁溶液)
D. 若电路中转移2mol电子,理论上有2molM从交换膜左侧向右侧迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、I等)中回收碘,其实验过程如下:
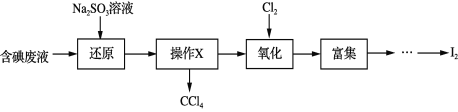
下列叙述不正确的是
A. “操作X”的名称为萃取,可在分液漏斗中进行
B. “还原”步骤发生的反应为:SO32+I2+H2O == 2I+SO42+2H+
C. “氧化”过程中,可用双氧水替代氯气
D. “富集”即I2富集于有机溶剂,同时除去某些杂质离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2014年11月,北京召开APEC会议,期间空气质量一级优,天空被称为“APEC蓝”。为了使“蓝天工程"可持续发展,下列做法正确的是( )
A.直接排放工业废气B.改进汽车尾气净化技术
C.采用焚烧方法处理垃圾D.过度开采和使用化石燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:
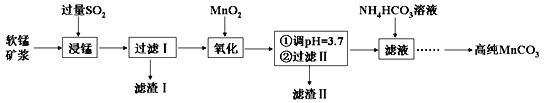
(1)过滤Ⅰ所得滤渣Ⅰ的主要成分为_________(填化学式)。
(2)“氧化”过程中除了发生MnO2与SO2的反应外,还发生另一氧化还原反应,写出该反应的离子方程式:__________________________。
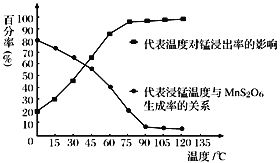
(3)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如右图所示,为减少 MnS2O6 的生成,“浸锰”的适宜温度是_______。
(4)向过滤Ⅱ所得的滤液中加入NH4HCO3 溶液时温度控制在30-35℃,温度不宜太高的原因是_______。
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有CO2气体生成,写出反应的离子方程式:_____________。
(6)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com