
 一定温度下在密闭容器内进行着某一反应,X气体,Y气体的物质的量 随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在密闭容器内进行着某一反应,X气体,Y气体的物质的量 随反应时间变化的曲线如图.下列叙述中正确的是( )| A. | 反应的化学方程式为2Y?X | B. | t1时,Y的浓度是X浓度的1.5倍 | ||
| C. | t2时,正、逆反应速率相等 | D. | t3时,逆反应速率大于正反应速率 |
分析 由图可知,X的物质的量增加,Y的物质的量减小,则Y为反应物、X为生成物,t3时,Y减少10mol-3mol=7mol,X增加5mol-2mol=3mol,t3时物质的量不再发生变化,则t3时达到平衡,反应为7Y?3X,以此来解答.
解答 解:A.物质的量的变化量之比等于速率之比,也等于化学计量数之比,t3时达到平衡,反应为7Y?3X,故A错误;
B.t1时,Y的浓度是X浓度的$\frac{6}{4}$=1.5倍,故B正确;
C.t2时,物质的量相等,但物质的量仍变化,正反应速率大于逆反应速率,故C错误;
D.t3时,达到平衡,逆反应速率等于正反应速率,故D错误;
故选B.
点评 本题考查物质的量浓度随时间的变化曲线,为高频考点,把握图中物质的量的变化、平衡判断、反应式的确定为解答的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 元素的非金属性C>A>B | |
| B. | C与A也可形成两种离子化合物 | |
| C. | 元素C、D、E形成的化合物溶于水后溶液呈中性 | |
| D. | 由C、E形成的化合物标准状况下不一定为气态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | B. | Na2CO3+CO2+H2O═2NaHCO3 | ||
| C. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | D. | NH4HS$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2S↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硬度高,热稳定性强 | B. | 耐热性好,耐磨性强 | ||
| C. | 导电性强,延展性好 | D. | 强度大,电绝缘性好 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气是氧化产物 | |
| B. | O2F2既是氧化剂又是还原剂 | |
| C. | 氧化剂与还原剂的物质的量之比为4:1 | |
| D. | 若生成4.48LHF,则转移0.8 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
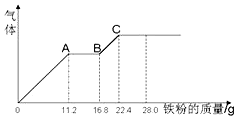 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A. | 原溶液中H2SO4浓度为4mol•L-1 | |
| B. | 图中,AB段的反应为2Fe3++Fe=3Fe2+,A点的溶质为Fe(NO3)3 | |
| C. | 原混合液中NO3-的物质的量为0.4mol | |
| D. | 图中,OA段产生是NO,BC段产生的气体是氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 研究化学反应中的能量变化有重要意义.请根据学过的知识回答下列问题:
研究化学反应中的能量变化有重要意义.请根据学过的知识回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在1L 0.1mol/L的Na2CO3溶液中,阴离子总数小于0.1NA | |
| B. | 将1 mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+数目为NA | |
| C. | 标准状况下,2.24L甲醇中含有C-H键的数目为0.3NA | |
| D. | 将1mol Cl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若Y(OH)n为强碱,则X(OH)n也一定为强碱 | |
| B. | 若HnXOm为强酸,则X的氢化物溶于水一定显酸性 | |
| C. | 若X元素形成的单质是X2,则Y元素形成的单质一定是Y2 | |
| D. | 若X的最高正价为+m,则Y的最高正价一定为+m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com