
����Ŀ����Ȼ���е����ʾ�������Ի�������ʽ���ڣ�Ϊ�˱����о������ã�����Ի������з�����ᴿ������A��B��C��D����ѧ�����Ļ���������ᴿ��װ�á�

I������ݻ���������ᴿ��ԭ�����ش�������ʵ������Ҫʹ������װ�á���A��B��C��D�����ʵ��Ŀո��С�
��1��̼�������Һ�з����̼���_____��
��2���Ȼ�����Һ�з�����Ȼ���____��
��3������ֲ���ͺ�ˮ____��
��4����ˮ����___��
��5����ȥ����ˮ�е�Cl��������____��
��6���ӵ�ˮ�з����I2____��
II����ˮ����ȡ�ⵥ�ʵķ������£�
��1����ȡ��Һ
�����п���Ϊ��ˮ����ȡ�ⵥ����ȡ������____
A���ƾ� B����
�ڷ�Һ©����ʹ��ǰ������____
�۲����ϵ�֪������H2O��>��������>�����ƾ��������â�����ѡ��ȡ����ȡ��ˮ�еĵⵥ�ʣ���Һʱ���ϲ�Һ����___ɫ��
��2������
��װ��A��a��������___��a�м�������___��ֹ����ʱҺ�屩�С�����װ��������ˮӦ��____�ڽ�����������������������
����֪������Ȼ�̼���۷е��������
�۵� | �е� | |
�� | 113.7�� | 184.3�� |
���Ȼ�̼ | -22.6�� | 76.8�� |
���������������Ȼ�̼�Ļ�����ƿ�����ռ��������ʵ�������______��
��ˮ���̲��ŷḻ����Դ����ʵ������ȡ������ˮ�������������̵�ʵ�飺
[��ˮ]![]() [����]
[����]![]() [ʳ��ˮ]��[�Ȼ��ƾ���]
[ʳ��ˮ]��[�Ȼ��ƾ���]
����һ�������к�Ca2+��Mg2+��SO42�������ʣ���Ҫ�ᴿ������ۺ����á������ᴿ�IJ����У�
�ټ��������Na2CO3��Һ �ڼ��������BaCl2��Һ �ۼ��������NaOH��Һ �ܵ�����Һ��pH����7 ���ܽ� ���� ����������ȷ�IJ���˳����____����ѡ����ĸ��
a���ݢڢۢ٢ޢܢ� b���ݢ٢ڢۢޢܢ�
c���ݢڢ٢ۢܢޢ� d���ݢۢڢ٢ޢܢ�
��������������е�____ʱ��ֹͣ���ȡ�
�������������к���������ɳ��CaCl2��MgCl2�������Σ��������ܽ���ȹ��˽���ɳ��ȥ���ټ�����Һ�е�SO42������μ���ijδ֪��Һ�е�SO42��___��
���𰸡�B D C A A C B ��© �Ϻ� ������ƿ ��ʯ�����Ƭ �� ���Ȼ�̼ ad ���������д���������� ȡ��������Һ�ڽྻ���Թ��У������е���������ϡ���ᣬ���������������μӼ����Ȼ�����Һ����������ɫ���������Һ�к������������֮���������
��������
I����ͼ��֪��װ��AΪ����װ�ã�װ��BΪ����װ�ã�װ��CΪ��Һװ�ã�װ��DΪ����װ�ã�
II����1�����ӵ�ˮ����ȡ�ⵥ�ʵ���ȡ��������ˮ���ܡ�������ˮ�͵ⷴӦ��������ȡ���е��ܽ��Զ����ˮ��
�����Һ©����ƿ���ͻ��������Է�Һ©����ʹ��ǰ�����ȼ���Ƿ�©Һ��
�������ܶȱ�ˮС��ѡ�ñ�����ȡ����ȡ��ˮ�еĵⵥ�ʣ��ϲ�Ϊ��ı���Һ��
��2����װ��AΪ����װ�ã�����ʱӦ��������ƿ�м����ʯ�����Ƭ��ֹ���У�Ϊ��ǿ����Ч��������װ��������ˮӦ�ô��¿ڽ���
�������������Ȼ�̼���۷е����ݿ�֪�����Ȼ�̼�ķе�ϵͣ�
��������һ����ȥ�����еĿ��������ʣ�����ѡ�ù�������������Һ��ȥMg2+�������Ȼ�����Һ��ȥSO42��������̼������Һ��ȥCa2+������Ba2+���������������Һ��pH����7��ȥ��������������̼������ӣ�
��������������е����������д����������ʱ��ֹͣ���ȣ������������ɣ�
������������ijδ֪��Һ�е�SO42���ķ������ȼ������ᣬ�ټ����Ȼ�����Һ���۲��Ƿ��а�ɫ�������ɡ�
I����1��̼�������Һ�з����̼���Ӧѡ�ù��˵ķ������ʴ�Ϊ��B��
��2���Ȼ�����Һ�з�����Ȼ���Ӧѡ�������ķ������ʴ�Ϊ��D��
��3������ֲ���ͺ�ˮӦѡ�÷�Һ�ķ������ʴ�Ϊ��C��
��4����ˮ����Ӧѡ������ķ������ʴ�Ϊ��A��
��5����ȥ����ˮ�е�Cl��������Ӧѡ������ķ������ʴ�Ϊ��A��
��6���ӵ�ˮ�з����I2Ӧѡ����ȡ��Һ�ķ������ʴ�Ϊ��C��
II����1�����ӵ�ˮ����ȡ�ⵥ�ʵ���ȡ��������ˮ���ܣ��ƾ��ܺ�ˮ������������ܣ���������ˮ����ѡB���ʴ�Ϊ��B��
�����Һ©����ƿ���ͻ��������Է�Һ©����ʹ��ǰ�����ȼ���Ƿ�©Һ���ʴ�Ϊ����©��
�������ܶȱ�ˮС��ѡ�ñ�����ȡ����ȡ��ˮ�еĵⵥ�ʣ��ϲ�Ϊ��ɫ���Ϻ�ɫ��ı���Һ���ʴ�Ϊ���Ϻ�ɫ��
��2����װ��AΪ����װ�ã�����a������Ϊ������ƿ��Ϊ��ֹ����ʱҺ�屩�У�Ӧ��������ƿ�м����ʯ�����Ƭ��ֹ���У�Ϊ��ǿ����Ч��������װ��������ˮӦ�ô��¿ڽ����ʴ�Ϊ��������ƿ����ʯ�����Ƭ���£�
�������������Ȼ�̼���۷е����ݿ�֪�����Ȼ�̼�ķе�ϵͣ����������������Ȼ�̼�Ļ�����ƿ�����ռ���������Ϊ���Ȼ�̼���ʴ�Ϊ�����Ȼ�̼��
��������һ����ȥ�����к�Ca2+��Mg2+��SO42��������ʱ��Ӧ�Ƚ������ܽ������Һ������Һ�м����������������Һ��ȥMg2+����������Ȼ�����Һ��ȥSO42���������������������Һ���Ȼ�����Һ��˳����Ե������ټ������̼������Һ��ȥCa2+������Ba2+�����ˣ�����Һ�м������������Һ��pH����7��ȥ��������������̼������ӣ��������������Һ�õ��Ȼ��ƾ��壬��ȷ�IJ���˳�����ݢڢۢ٢ޢܢ����ݢۢڢ٢ޢܢ����ʴ�Ϊ��ad��
��������������е����������д����������ʱ��ֹͣ���ȣ������������ɣ��ʴ�Ϊ�����������д���������֣�
������������ijδ֪��Һ�е�SO42���ķ�����ȡ��������Һ�ڽྻ���Թ��У������е���������ϡ���ᣬ�������������μӼ����Ȼ�����Һ���۲��Ƿ������ɫ�������ʴ�Ϊ��ȡ��������Һ�ڽྻ���Թ��У������е���������ϡ���ᣬ�������������μӼ����Ȼ�����Һ����������ɫ���������Һ�к������������֮���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�������Ҫ�Ļ���ԭ�ϣ��ֿ���Ϊȼ�ϡ�����CO2��H2�ڴ����������ºϳɼ״�����Ҫ�����ķ�Ӧ���£�
��Ӧ����CO2(g)+3H2(g)CH3OH(g)+H2O(g) H1=-53.7 kJmol-1
��Ӧ����CO2(g)+H2(g)CO(g)+H2O(g) H2=+41.2 kJmol-1
(1)��֪��ѧ���ļ������£�

�ٷ�Ӧ����CO(g)+ 2H2(g) CH3OH(g) H3=_____________��
��̼��˫���ļ���Ϊ__________________��
����ijһ�����£�������Ӧͬʱ����������ӦI����III�Ļ�ѧƽ�ⳣ���ֱ�ΪK1��K2��K3����K2=____________________(�ú�K1��K3����ʽ��ʾ)��
(2)�о��������ڴ��������£�CO2��H2�ɷ�����ӦI�͢�ijʵ���ҿ���CO2��H2��ʼͶ�ϱ�Ϊ1��2��2��������ͬ��Ӧʱ��������ʵ������(�״�ѡ���Լ�ת����CO2�����ɼ״��İٷ���)��
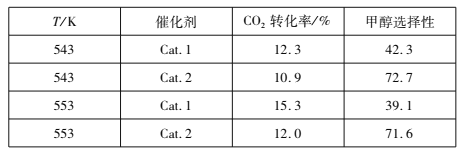
��543 Kʱ��ʹ�ô���Cat��2�����ʵ������ʱ��ӦI������״̬Ϊ________________(���������С�����ƽ��״̬������������С�)��
����������߷�ӦI��H2ƽ��ת���ʵĴ�ʩ��___________(����)��
A��ʹ�ô���Cat��1 B�����ͷ�Ӧ�¶�
C��Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ�� D����СCO2��H2�ij�ʼͶ�ϱ�

(3)��������Ӧ�У��������CO��CO2��H2����ɹ�ϵΪn(H2)��n(CO+ CO2)=2.60ʱ����ϵ�е�COƽ��ת���ʦ�(CO)���¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
��ͼ�е�ѹǿ�ɴ�С��˳��Ϊ____________��
�ڦ�(CO)ֵ���¶����߶���С��ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaClO2��һ����Ҫ��ɱ����������Ҳ������Ư��֯��ȣ���һ�������������£�
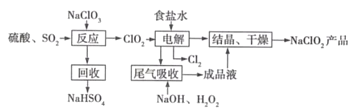
�ش��������⣺
��1��NaClO2��Cl�Ļ��ϼ�Ϊ_______��
��2��д������Ӧ������������ClO2�Ļ�ѧ����ʽ_______��
��3�������������ʳ��ˮ�ɴ���ˮ���ƶ��ɣ�����ʱ��Ϊ��ȥMg2+��Ca2+��Ҫ������Լ��ֱ�Ϊ________��________�����������������Ӧ����Ҫ������______��
��4����β��������������������������ų�������ClO2�������շ�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ________���÷�Ӧ������������_________��
��5������Ч�Ⱥ��������������������������������������䶨���ǣ�ÿ�˺��������������������൱�ڶ��ٿ�Cl2������������NaClO2����Ч�Ⱥ���Ϊ____����������������λС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��2����ѧ�뼼��]
�ۺ���������PFS����˭��������Ҫ������������ͼ���Ի��շ���мΪԭ���Ʊ�PFS��һ�ֹ������̡�

�ش���������
��1������м��ҪΪ���渽�д�������������������Ҫ�ɷ�Ϊ_________�������ɸ��Ŀ����_______
��2�����ʱ����ʵ�����_____��д���������ᷴӦ�����ӷ���ʽ_____________________��
��3����Ӧ���м�����������������_________������������������ʵ���____________�����ţ���
A��KMnO4 | B�� | C�� | D�� |
��4���ۺϸ�����Һ��pH���������һ���ķ�Χ�ڣ�pHƫСʱFe3+ˮ��̶�����pHƫ��ʱ��_______��
��5������ڳ�ѹ��������ѹ�������ŵ���______��
��6���λ���B�Ǻ�������������Ч������Ҫָ�꣬����ʽΪ![]() ��nΪ���ʵ�������Ϊ������Ʒ��Bֵ��ȡ��Ʒmg��ȷ����������ᣬ��ַ�Ӧ���ټ�����к���ȴ������ˮ���Է�̪Ϊָʾ������c
��nΪ���ʵ�������Ϊ������Ʒ��Bֵ��ȡ��Ʒmg��ȷ����������ᣬ��ַ�Ӧ���ټ�����к���ȴ������ˮ���Է�̪Ϊָʾ������c![]() �ı�NaOH��Һ�����к͵ζ������ֲ�����ȥ�����ų������Ӹ��ţ������յ�ʱ����NaOH��ҺV mL�����������������հ������飬����NaOH��Һ
�ı�NaOH��Һ�����к͵ζ������ֲ�����ȥ�����ų������Ӹ��ţ������յ�ʱ����NaOH��ҺV mL�����������������հ������飬����NaOH��Һ![]() ����֪����Ʒ��Fe����������w����B�ı���ʽΪ__________
����֪����Ʒ��Fe����������w����B�ı���ʽΪ__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�����ʵ����ʵ���Ũ��Ϊ1mol/L���ǣ� ��
A. ��58.5g NaCl�ܽ���1Lˮ��
B. ��1L 10mol/L���������9Lˮ��
C. ��11.2L HCl��������ˮ���0.5L��Һ
D. ��40g NaOH�ܽ�������ˮ�У��ټ�����ˮֱ����Һ���Ϊ1L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��5���л���ѧ����]��Ȳ���ڴ��������¿ɷ���ż����Ӧ����ΪGlaser��Ӧ��
2R��C��C��H![]() R��C��C��C��C��R+H2
R��C��C��C��C��R+H2
�÷�Ӧ���о����ͷ�����ϡ������ӻ�ѧ�ȷ��������Ҫ��ֵ������������Glaser��Ӧ�Ʊ�������E��һ�ֺϳ�·�ߣ�

�ش��������⣺
��1��B�Ľṹ��ʽΪ______��D �Ļ�ѧ����Ϊ______��
��2���������ķ�Ӧ���ͷֱ�Ϊ______��______��
��3��E�Ľṹ��ʽΪ______����1 mol E�ϳ�1,4���������飬��������Ҫ��������_______mol��
��4�������![]() ��Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
��Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
��5�����㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3:1��д������3�ֵĽṹ��ʽ_______________________________��
��6��д����2�����Ҵ�Ϊԭ�ϣ��������Լ���ѡ���Ʊ�������D�ĺϳ�·��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����мס��ҡ�������ͬѧ�ֱ����Fe��OH��3������Ʊ�ʵ�飮
I����ͬѧ��1molL��1�Ȼ�����Һ�м���������NaOH��Һ��
II����ͬѧֱ�Ӽ��ȱ���FeCl3��Һ��
III����ͬѧ��25ml��ˮ����μ���5��6��FeCl3������Һ�������������Һ�ʺ��ɫ��ֹͣ���ȣ� �Իش��������⣺
��1�����в�����ȷ��ͬѧ��_____��д���˹����еĻ�ѧ����ʽ��_____________��
��2��֤����Fe��OH��3�������ɵ����ʵ�������___________________________��
��3��Fe��OH��3�����Dz��ǵ���ʣ�_____ ����ǡ����ǡ�����
��4����ͬѧ�������Ƶõ�Fe��OH��3�����������ʵ�飺
�ٽ���װ��U�ι��ڣ���ʯī���缫����ֱͨ���磬ͨ��һ��ʱ�����������������ɫ��������Fe��OH��3������_____��ɣ�
�������м��뱥��Na2SO4��Һ��������������_________________________________��
��������Fe��OH��3��������εμ�������Һ����ʼ�������ɫ������������Ϊ_____�������μӣ�����������ʧ�ҵ��ػ�ɫ��Һ��д����ѧ����ʽ______________________��
������ȥFe��OH��3�����л��е�NaCl������������Ʒ��_____������������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪KMnO4��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��2KMnO4+16HCl��Ũ����2MnCl2+8H2O+2KCl+5Cl2�����ش��������⣺
��1������˫���ű�ʾ���÷�Ӧת�Ƶ��ӵķ������Ŀ_______________________________
��2����������HClռHCl������_______ ����ԭ��Ԫ��_________����Ԫ�ط��ţ�
��3������״������0.5mol��������ʱ���÷�Ӧת�Ƶĵ�����Ϊ_____����NAΪ�����ӵ�������ֵ��
��4��15.8g KMnO4�뺬1.2molHCl��Ũ������ȫ��Ӧ������HCl�ӷ������ڷ�Ӧ�����Һ�м���������AgNO3��Һ��������_____g������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭҺ�������һ�ֵͳɱ��Ĵ��ܵ�أ���ؽṹ��ͼ��ʾ������ԭ��ΪFe3++Cr2+![]() Fe2++Cr3+������˵����ȷ����
Fe2++Cr3+������˵����ȷ����

A. ��س��ʱ��b���ĵ缫��ӦʽΪCr3++e-=Cr2+
B. ��س��ʱ��Cl-��a������ѡ������Ĥ����b��
C. ��طŵ�ʱ��a���ĵ缫��ӦʽΪFe3++3e-=Fe
D. ��طŵ�ʱ����·��ÿͨ��0. 1 mol���ӣ�Fe3+Ũ�Ƚ���0. 1 mol��L-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com