
| A. | 一定含有Mg2+、Al3+、Clˉ,可能含有Na+,不含NH4+ | |
| B. | 一定含有Mg2+、Clˉ,不含NH4+,可能含有Na+、Al3+ | |
| C. | c (Clˉ) 为 4.00 mol•L-1,c(Al3+)为5.00 mol•L-1 | |
| D. | c (Mg2+) 为 1.00 mol•L-1,c(Na+)为 0.5mol•L-1 |
分析 ①加入NaOH溶液加热,有白色沉淀产生,无刺激气味气体生成,说明原溶液中可能含有Mg2+、Al3+,一定没有NH4+;滤液中c(OH-)=0.2mol•L-1,证明碱过量,一定含有Mg2+;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48g,溶液中一定含有Cl-;
氢氧化镁1.16g,物质的量是$\frac{1.16g}{58g/mol}$=0.02mol,消耗的n(OH-)=0.04mol,加入的氢氧化钠为0.025L×4mol/L=0.1molmol,滤液中的n(OH-)=0.2mol•L-1×0.1L=0.02mol,故Al3+消耗了0.04mol氢氧化钠生成偏铝酸钠,n(Al3+)=0.01mol,生成白色沉淀11.48g是氯化银,物质的量是0.08mol,氢氧化镁有0.02mol,n(Al3+)=0.01mol,根据电荷守恒,n(Na+)=n(Cl-)-2n(Mg2+)-3n(Al3+),以此来解答.
解答 解:①加入NaOH溶液加热,有白色沉淀产生,无刺激气味气体生成,说明原溶液中可能含有Mg2+、Al3+,一定没有NH4+;滤液中c(OH-)=0.2mol•L-1,证明碱过量,一定含有Mg2+;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48g,溶液中一定含有Cl-;
氢氧化镁1.16g,物质的量是$\frac{1.16g}{58g/mol}$=0.02mol,消耗的n(OH-)=0.04mol,加入的氢氧化钠为0.025L×4mol/L=0.1molmol,滤液中的n(OH-)=0.2mol•L-1×0.1L=0.02mol,故Al3+消耗了0.04mol氢氧化钠生成偏铝酸钠,n(Al3+)=0.01mol,生成白色沉淀11.48g是氯化银,物质的量是$\frac{11.48g}{143.5g/mol}$=0.08mol,氢氧化镁有0.02mol,n(Al3+)=0.01mol,根据电荷守恒,n(Na+)=n(Cl-)-2n(Mg2+)-3n(Al3+)=0.01mol,
A.根据以上分析可知,溶液中一定存在:Na+、Mg2+、Al3+、Cl-,由于一定含有Na+,故A错误;
B.溶液中一定存在:Na+、Mg2+、Al3+、Cl-,即一定含有Al3+,故B错误;
C.c(Al3+)=$\frac{0.01mol}{0.02L}$=0.5 mol•L-1,c(Cl-)=$\frac{0.08mol}{0.02L}$=4mol/L,故C错误;
D.c(Mg2+)=$\frac{0.02mol}{0.02L}$=1.00 mol•L-1,c(Na+)=$\frac{0.01mol}{0.02L}$=0.50 mol•L-1,故D正确;
故选D.
点评 本题考查离子反应的计算及推断,为高频考点,把握沉淀的成分、离子检验及电荷守恒应用等为解答的关键,侧重分析、推断、计算能力的综合考查,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | 向FeCl2溶液中滴入氯水2Fe2++Cl2═2Fe3++2Cl- | 向FeCl2溶液中滴入碘水2Fe2++I2═2Fe3++2I- |
| B | CO2通入漂白粉溶液中CO2+Ca2++2ClO-+H2O═CaCO3↓+2HClO | SO2通入漂白粉溶液中SO2+Ca2++2ClO-+H2O═CaSO3↓+2HClO |
| C | 向Na2CO3溶液中滴入稀HNO3CO32-+2H+═CO2↑+H2O | 向Na2SO3溶液中滴入稀HNO3SO32-+2H+═SO2↑+H2O |
| D | 向澄清石灰水中通入少量CO2 气体Ca2++2OH-+CO2═CaCO3↓+H2O | 向澄清石灰水中通入少量SO2 气体Ca2++2OH-+SO2═CaSO3↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入2mol.L-l的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入2mol.L-l的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )| A. | 反应前的溶液中,硝酸的物质的量为0.2 mol | |
| B. | C点对应NaOH溶液的体积为48 mL | |
| C. | 样品中铝粉和铁粉的物质的量之比为5:3 | |
| D. | D点与A点沉淀物质的量的差为0.02 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
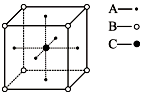 (1)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体类型为分子晶体.
(1)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体类型为分子晶体. 、④CH3-CH3这四种分子中碳原子采取sp2杂化的是①③(填序号).
、④CH3-CH3这四种分子中碳原子采取sp2杂化的是①③(填序号).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水电离产生的H+浓度为1×10-12mol•L-1的溶液:NH4+、Na+、Cl-、CO32- | |
| B. | 能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- | |
| C. | 0.1 mol/L的NaNO3溶液中:H+、Fe2+、Cl-、SO42- | |
| D. | 含有大量Al3+的水溶液中:Na+、NH4+、HCO3-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 共价化合物中各原子最外层都一定满足8电子结构 | |
| B. | BaO2晶体中阳离子与阴离子数目之比为1:2 | |
| C. | H2O是一种非常稳定的化合物,这是由氢键所致 | |
| D. | 在反应2Na2O2+2H2O═4NaOH+O2↑中,既有离子键、极性键和非极性键的断裂,又有离子键、极性键和非极性键的形成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com