
分析 根据将盐溶液蒸干时盐水解出的酸和碱的性质来分析盐的水解能否进行彻底:
若盐水解出的是强碱和弱酸,由于有强碱生成,则弱酸很难挥发除去,则水解不能彻底;
若盐水解出的是弱碱和不挥发的强酸,则由于强酸不挥发,则水解不能彻底;
若盐水解出的是弱碱和挥发性或易分解的酸,则酸的挥发或分解导致水解被促进,则能进行彻底,据此分析.
解答 解:AlCl3 水解生成Al(OH)3和HCl,由于Al(OH)3是弱碱,而HCl是挥发性酸,HCl的挥发会导致水解被促进,则蒸干后的到的是Al(OH)3;
Al2(SO4)3 水解为Al(OH)3和硫酸,但硫酸是不挥发性酸,加热时不挥发,故水解不彻底,得到的仍然是Al2(SO4)3;
FeCl3 水解生成Fe(OH)3和HCl,由于Fe(OH)3是弱碱,而HCl是挥发性酸,HCl的挥发会导致水解被促进,则蒸干后的到的是Fe(OH)3;
Na2CO3 水解生成NaOH和碳酸,但由于氢氧化钠是强碱,故碳酸很难挥发或分解,故得到的仍然是Na2CO3;
CuSO4水解为Cu(OH)2和硫酸,但硫酸是不挥发性酸,加热时不挥发,故水解不彻底,得到的仍然是CuSO4;
故答案为:Al(OH)3;Al2(SO4)3;Fe(OH)3; Na2CO3;CuSO4.
点评 本题考查盐类水解的应用,为高频考点,侧重学生的分析能力的考查,题目难度不大,注意盐类水解的原理,特别是能把握相关物质的性质.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
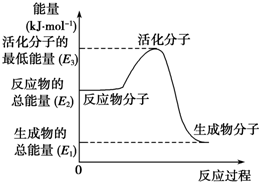 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是| A. | 上述图示的反应为吸热反应 | |
| B. | 图中的能量变化如图所示,则△H=E1-E3 | |
| C. | H2燃烧能放出大量的热,故CH3OH转变成H2的过程必须吸收热量 | |
| D. | 根据①②推知:在25℃、101 kPa时,1 mol CH3OH(g)完全燃烧生成CO2和H2O放出的热量应大于676.7 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温常压下,1mol Mg与足量盐酸反应失去电子数为2NA | |
| B. | 标准状况下,11.2L H2O所含的分子数为0.5NA | |
| C. | 0.1molCH4所含的电子数为NA | |
| D. | 通常状况下,NA 个CO2分子占有的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 96% | B. | 48% | C. | 9.6% | D. | 56% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 3:2 | D. | 6:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有O2 | B. | 肯定只有NH3和NO | ||
| C. | 肯定有NH3、NO、HCl | D. | 肯定没有Cl2、NH3、NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 ;
; +O2$→_{△}^{Cu}$OHCCHO+2H2O;
+O2$→_{△}^{Cu}$OHCCHO+2H2O;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com