

·ÖĪö £Ø1£©Ķ¼ÖŠĖłĖµµÄ”°¼ī”±ĪŖ“æ¼ī£¬¼“Ģ¼ĖįÄĘ£»
£Ø2£©¶”ÖŠĢ¼ĖįÄĘÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆÄĘ”¢Ė®”¢¶žŃõ»ÆĢ¼£»
£Ø3£©ĒāŃõ»ÆĀĮŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆĀĮŗĶĖ®£»
£Ø4£©ĀČ»ÆøĘÓėĢ¼ĖįÄĘ·“Ӧɜ³É³Įµķ£¬¶ųĢ¼ĖįĒāÄĘ²»ÄÜ£¬æɼų±š£»
£Ø5£©FeÓėĀČ»ÆĢś·“Ӧɜ³ÉĀČ»ÆŃĒĢś£®
½ā“š ½ā£ŗ£Ø1£©Ķ¼ÖŠĖłĖµµÄ”°¼ī”±ĪŖ“æ¼ī£¬¼“Ģ¼ĖįÄĘ£¬Ęä»ÆѧŹ½ĪŖNa2CO3£¬¹Ź“š°øĪŖ£ŗNa2CO3£»
£Ø2£©¶”ÖŠĢ¼ĖįÄĘÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆÄĘ”¢Ė®”¢¶žŃõ»ÆĢ¼£¬Ąė×Ó·“Ó¦ĪŖCO32-+2H+=CO2”ü+H2O£¬¹Ź“š°øĪŖ£ŗCO32-+2H+=CO2”ü+H2O£»
£Ø3£©ĒāŃõ»ÆĀĮŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆĀĮŗĶĖ®£¬Ąė×Ó·“Ó¦ĪŖAl£ØOH£©3+3H+=Al3++3H2O£¬¹Ź“š°øĪŖ£ŗAl£ØOH£©3+3H+=Al3++3H2O£»
£Ø4£©ĀČ»ÆøĘ£Ø»ņĀČ»Æ±µ£©ÓėĢ¼ĖįÄĘ·“Ӧɜ³É³Įµķ£¬¶ųĢ¼ĖįĒāÄĘ²»ÄÜ£¬æɼų±š£¬·¢ÉśµÄĄė×Ó·“Ó¦ĪŖCO32-+Ca2+=CaCO3”ż£Ø»ņCO32-+Ba2+=BaCO3”ż£©£¬¹Ź“š°øĪŖ£ŗCO32-+Ca2+=CaCO3”ż£Ø»ņCO32-+Ba2+=BaCO3”ż£©£»
£Ø5£©FeÓėĀČ»ÆĢś·“Ӧɜ³ÉĀČ»ÆŃĒĢś£¬Ąė×Ó·“Ó¦ĪŖ2Fe3++Fe=3Fe2+£¬¹Ź“š°øĪŖ£ŗ2Fe3++Fe=3Fe2+£®
µćĘĄ ±¾Ģāæ¼²éĄė×Ó·“Ó¦·½³ĢŹ½µÄŹéŠ“£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ·¢ÉśµÄ·“Ó¦¼°Ąė×Ó·“Ó¦µÄŹéŠ“·½·ØĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲø“·Ö½ā·“Ó¦µÄĄė×Ó·“Ó¦¼°·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
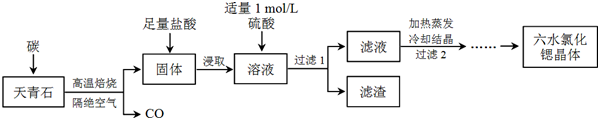
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °±Ė®ÓėĻ”ŃĪĖį·“Ó¦£ŗH++OH-ØTH2O | |
| B£® | FeCl3ČÜŅŗÓėĢś·“Ó¦£ŗFe3++FeØT2Fe2+ | |
| C£® | Fe3O4ČÜÓŚ×ćĮæĻ”HNO3£ŗFe3O4+8H+ØTFe2++2Fe3++4H2O | |
| D£® | KOHĻ”ČÜŅŗÖŠĶØČė¹żĮæµÄSO2£ŗSO2+OH-ØTHSO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
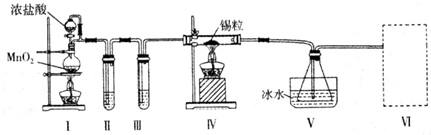
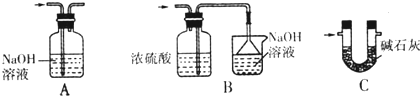
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
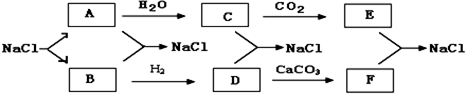
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĖįÓźÄÜŹ¹øÖĢśøüČŻŅ×·¢Éśµē»ÆѧøÆŹ“ | |
| B£® | øÖĢśŌŚ³±ŹŖµÄµŲŅ¤ÖŠ½ĻŅ×·¢ÉśĪöĒāøÆŹ“ | |
| C£® | ĢśŠāµÄÖ÷ŅŖ³É·ÖŹĒFe2O3•nH2O | |
| D£® | øÖĢśŠāŹ“Ź±£¬ĢśŌ×ÓŹ§Č„µē×Ó³ÉĪŖFe3+£¬¶ųŗóÉś³ÉFe£ØOH£©3£¬ŌŁ²æ·ÖĶŃĖ®³ÉĪŖŃõ»ÆĢśµÄĖ®ŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com