
美国麻省理工学院的丹尼尔·诺切拉博士公布了自己团队研发的“人造树叶”,它可以与燃料电池共同构成一个新的发电装置——太阳能燃料电池,工作原理如图所示,下列有关叙述正确的是( )
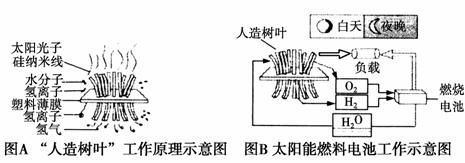
A.“人造树叶”上发生的反应为6CO2+6H2O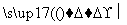 C6H12O6+6O2
C6H12O6+6O2
B.图A中塑料薄膜上部的反应为2H++2e-===H2↑
C.图B燃料电池工作时的负极反应物为O2
D.太阳能燃料电池的优点为无论天气如何,均能持续供应电能,并且实现对环境的“零排放”
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):NN为942、OO为500、NN为154,则断裂1 mol NH键所需的能量(kJ)是( )

A.194 B.391
C.516 D.658
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
B.25 ℃、101 kPa时,1 mol S和2 mol S的燃烧热不相等
C.通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能
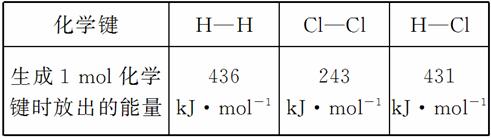
则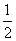 H2(g)+
H2(g)+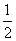 Cl2(g)===HCl(g) ΔH=-183 kJ·mol-1
Cl2(g)===HCl(g) ΔH=-183 kJ·mol-1
D.任何化学反应都伴随着能量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.把a L 0.1 mol·L-1的CH3COOH溶液与b L 0.1 mol·L-1的KOH溶液混合,所得溶液中一定存在:c(K+)+c(H+)=c(CH3COO-)+c(OH-)
B.把0.1 mol·L-1的NaHCO3溶液与0.3 mol·L-1的Ba(OH)2溶液等体积混合,所得溶液中一定存在:c(OH-)>c(Ba2+)>c(Na+)>c(H+)
C.向1 mol·L-1的CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高
D.常温下,在pH=3的CH3COOH溶液和pH=11的NaOH溶液中,水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25 ℃时,有关物质的电离平衡常数如下表所示:
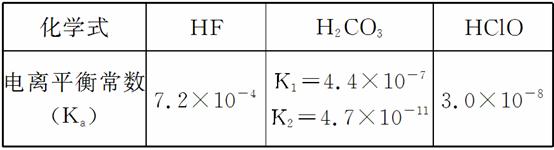
(1)将浓度为0.1 mol·L-1 HF溶液加水稀释一倍(假设温度不变),下列各量增大的是________。
A.c(H+) B.c(H+)·c(OH-)
C.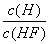 D.
D.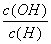
(2)25 ℃时,在20 mL 0.1 mol·L-1氢氟酸中加入V mL 0.1 mol·L-1 NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是________。
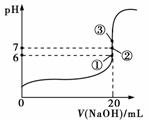
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中c(F-)-c(Na+)=9.9×10-7 mol·L-1
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20 mL,此时溶液中c(F-)<c(Na+)=0.1 mol·L-1
(3)物质的量浓度均为0.1 mol·L-1的下列四种溶液:①Na2CO3溶液;②NaHCO3溶液;③NaF溶液;④NaClO溶液。依据数据判断pH由大到小的顺序是__________________。
(4)Na2CO3溶液显碱性是因为CO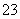 水解的缘故,请设计简单的实验事实证明之__________________。
水解的缘故,请设计简单的实验事实证明之__________________。
(5)长期以来,一直认为氟的含氧酸不存在。1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H—O—F。HFO与水反应得到HF和化合物A,每生成1 mol HF转移________mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
盐酸和K2CO3反应时,能使反应的最初速率明显加快的是( )
A.将盐酸用量增加一倍 B.盐酸的浓度增加一倍,用量减半
C.温度升高30 ℃ D.增加K2CO3粉末的量
查看答案和解析>>
科目:高中化学 来源: 题型:
在0.1 mol·L-1明矾溶液100 mL中,加入0.1 mol·L-1的Ba(OH)2溶液,当SO42-恰好沉淀完全时,同时得到的氢氧化铝的物质的量为( )。
A.0.01 mol B.0.005 mol C.0.0133 mol D.0 mo1
查看答案和解析>>
科目:高中化学 来源: 题型:
t℃,水的离子积为KW,该温度下将a mol/L一元酸HA与b mol/L一元碱BOH等体积积混合,要使混合液呈中性,必要的条件是( )
A.混合液中c(H+)=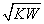
B.混合液的pH=7
C.a=b
D.混合液中c(B+)=c(A-)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com