
在恒温恒容容器中进行反应A(g)  2B(g)+C(g),若A的浓度由0.1 mol·L
2B(g)+C(g),若A的浓度由0.1 mol·L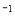 降到0.06 mol·L
降到0.06 mol·L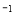 需20 s,那么由0.06 mol·L
需20 s,那么由0.06 mol·L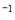 降到0.024 mol·L
降到0.024 mol·L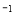 需要的时间
需要的时间
A.等于18s B,等于12s C,小于18s D.大于18s
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:2013-2014河南省高二下学期期中考试化学试卷(解析版) 题型:选择题
某有机物的结构简式如图,它在一定条件下能发生下列哪些反应( )

①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去
A.②③④ B.①③⑤⑥ C.①③④⑤ D.②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省濮阳市高二下学期升级考试化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.石油分馏、煤的干馏均是物理变化
B.PM2.5是指氮、硫的氧化物溶于水形成的酸性液体造成的空气污染
C.可利用清洁能源如太阳能、潮汐能、风能来发电
D.铅蓄电池、锂电池、碱性锌锰干电池都属于二次电池
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省濮阳市高一下学期升级考试化学(A卷)试卷(解析版) 题型:填空题
实验室用碳酸钠晶体配制1.00 mol/L的溶液l00mL,回答下列问题:
(1)所需主要仪器为:药匙、托盘天平、烧杯、量筒________、________和胶头滴管;
(2)本实验须称量碳酸钠晶体(Na2CO3.10H2O)________g。
(3)容量瓶上标有:____________、____________、____________。
(4)某同学将称量好的碳酸钠晶体用适量的蒸馏水在烧杯中溶解,冷却后直接倒进所选的且经检查不漏水的容量瓶中,洗涤烧杯2—3次,洗涤液也移至容量瓶中,晃动容量瓶使其混合均匀,然后加水至离刻度线2cm处,用胶头滴管加水至刻度线,倒入试剂瓶贴上标签备用。请指出上述操作中的两处明显错误:______________________;
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省濮阳市高一下学期升级考试化学(A卷)试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.向NH4HCO3溶液中加过量Ca(OH)2溶液:HCO3-+OH-+Ca2+=CaCO3↓+H2O
B.用惰性电极MgCl2电解水溶液:2Cl-+2H2O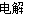 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.向偏铝酸钠溶液中加入少量硫酸氢钠溶液:2AlO2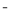 +H
+H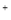 +H2O=Al(OH)3↓
+H2O=Al(OH)3↓
D.浓盐酸跟二氧化锰混合共热:MnO2+4H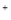 +4Cl
+4Cl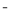 =Mn
=Mn +2H2O+2Cl2↑
+2H2O+2Cl2↑
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省濮阳市高一下学期升级考试化学(A卷)试卷(解析版) 题型:选择题
下列说法不正确的是
A.在共价化合物中一定含有共价键
B.含有离子键的化合物一定是离子化合物
C.含有共价键的化合物一定是共价化合物
D.化学反应过程中,反应物分子内的化学键断裂,产物分子的化学键形成
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省濮阳市高一下学期升级考试化学(A卷)试卷(解析版) 题型:选择题
下列说法不正确的是
A.大气污染物主要来自化石燃料和工业生产过程产生的废气
B.形成酸雨的主要物质是硫氧化物和氮氧化物(NOx)
C.绿色化学的核心就是在生产过程中减少污染
D.水华、赤潮等水体污染是由于含氮、磷的大量污水任意排放造成的
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省洛阳市高三年级第三次考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 垃圾资源化的主要途径是卫生填埋
B. 在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因
C. 推广使用新能源,可以减少二氧化碳等温室气体的排放
D. 人造纤维、合成纤维和光导纤维都是有机高分子化合物
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省高二上学期期末考试化学试卷(解析版) 题型:实验题
用中和滴定的方法测定NaOH和Na2CO3的混合溶液中NaOH的含量,可先在混合液中加入过量的BaCl2溶液,使Na2CO3完全转变成BaCO3沉淀,然后用标准盐酸滴定(已知几种酸碱指示剂变色的pH范围:①甲基橙3.1~4.4 ②甲基红4.4~6.2 ③酚酞8.2~10)。请回答:
(1)向混有BaCO3沉淀的NaOH溶液中滴入盐酸,应选用 指示剂,判断到达滴定终点的实验现象是 。
(2)为测定某烧碱样品中NaOH的含量(设样品中杂质为Na2CO3),某同学进行如下实验:准确称取5.0g样品配制成250mL溶液,然后分三次各取配制好的烧碱溶液20.00mL于三个用蒸馏水洗净的锥形瓶中,分别加入过量的BaCl2溶液,并向锥形瓶中各加入1~2滴指示剂,用浓度为0.2000mol·L-1的盐酸标准液进行滴定,相关数据记录如下:
实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
初读数 | 末读数 | ||
1 | 20.00 | 0.00 | 31.00 |
2 | 20.00 | 1.00 | 32.04 |
3 | 20.00 | 1.10 | 32.18 |
①实验3到达滴定终点时所耗HCl溶液的体积为 ;依据表中数据,计算出烧碱样品中含NaOH的质量分数为 %。(小数点后保留两位数字)
②滴定时的正确操作是 。
③下列操作会导致烧碱样品中NaOH含量测定值偏高的是
A.锥形瓶用蒸馏水洗后未用待测液润洗 B.酸式滴定管用蒸馏水洗后未用标准液润洗
C.在滴定前有气泡,滴定后气泡消失 D.滴定前平视读数,滴定结束俯视读数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com