
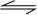 CH3OH��g�������ʵ������١�n
CH3OH��g�������ʵ������١�n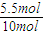 =0.55��
=0.55��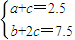 �����2a+2.5=b��
�����2a+2.5=b��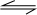 CH3OH��g����
CH3OH��g����


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �¶�/�� | 250 | 310 | 350 |
| K | 2.041 | 0.250 | 0.012 |
| Ũ��mol/L ʱ��/min |
c��CO�� | c��H2�� | c��CH3OH�� |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | 1.2 | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ��㶫ʡ��ɽ�и߶���ѧ����ĩ���Ի�ѧ�Ծ����������� ���ͣ������
��15�֣�������һ����Ҫ�Ļ���ԭ�ϣ����������������ء�����̬�����Լ����ᣬ���л��ϳɹ�ҵ���ƺϳ���ά�����ϡ�Ⱦ�ϵȡ���ش��������⣺
��1�������ǹ�ҵ�Ʊ��������Ҫԭ�ϣ���֪���������Ȼ�ѧ����ʽ��
�� N2 (g)+ 3H2 (g) 2NH3 (g) ��H1
2NH3 (g) ��H1
�� 4NH3(g) +5O2 (g)�� 4NO(g) +6H2O(l) ��H2
�� N2 (g)+ O2 (g)�� 2NO (g) ��H
�ܷ�Ӧ�á�H1�͡�H2��ʾ��H��
�����á�H1�͡�H2��ʾ��H����д����H= �������ܣ�˵�����ɣ�
��
��2������ͬ���¶��£��ݻ���ȵ����������ܱ���������ŷֱ�Ϊa��b���У�һ�����ĵ����������������п��淴Ӧ��
N2(g) �� 3H2(g)  2NH3(g) ��H����92.4 kJ/mol
2NH3(g) ��H����92.4 kJ/mol
ʵ���÷�Ӧ��ʼʱ�����ʵ����ʵ�����ƽ��ʱ�ų����������±���
| ������� | ��ʼʱ���������ʵ���/mol | ƽ��ʱ��Ӧ | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | 23.1 |
| b | 2 | 6 | 0 | δ֪����E��ʾ�� |
 2NH3(g) ��H��0 ��
2NH3(g) ��H��0 ��
 CH3OCH3(g)��3H2O(g) ��H��0
CH3OCH3(g)��3H2O(g) ��H��0| ���� | c(CO2) /mol��L��1 | c(H2) /mol��L��1 | c(CH3OCH3) /mol��L��1 | c(H2O) /mol��L��1 | v (��)��v (��)�Ƚ� |
| ����I | 1.0��10��2 | 1.0��10��2 | 1.0��10��4 | 1.0��10��4 | v (��)��v (��) |
| ����II | 2.0��10��2 | 1.0��10��2 | 1.0��10��4 | 2.0��10��4 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��㶫ʡ��ɽ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��15�֣�������һ����Ҫ�Ļ���ԭ�ϣ����������������ء�����̬�����Լ����ᣬ���л��ϳɹ�ҵ���ƺϳ���ά�����ϡ�Ⱦ�ϵȡ���ش��������⣺
��1�������ǹ�ҵ�Ʊ��������Ҫԭ�ϣ���֪���������Ȼ�ѧ����ʽ��
�� N2 (g)+ 3H2
(g)  2NH3 (g) ��H1
2NH3 (g) ��H1
�� 4NH3(g) +5O2 (g)�� 4NO(g) +6H2O(l) ��H2
�� N2 (g)+ O2 (g)�� 2NO (g) ��H
�ܷ�Ӧ�á�H1�͡�H2��ʾ��H��
�����á�H1�͡�H2��ʾ��H����д����H= �������ܣ�˵�����ɣ�
��
��2������ͬ���¶��£��ݻ���ȵ����������ܱ���������ŷֱ�Ϊa��b���У�һ�����ĵ����������������п��淴Ӧ��
N2(g)
�� 3H2(g)
 2NH3(g) ��H����92.4 kJ/mol
2NH3(g) ��H����92.4 kJ/mol
ʵ���÷�Ӧ��ʼʱ�����ʵ����ʵ�����ƽ��ʱ�ų����������±���
|
������� |
��ʼʱ���������ʵ���/mol |
ƽ��ʱ��Ӧ |
||
|
N2 |
H2 |
NH3 |
||
|
a |
1 |
3 |
0 |
23.1 |
|
b |
2 |
6 |
0 |
δ֪����E��ʾ�� |
����˵����ȷ���� ������ţ�
�� ��Ӧa�ͷ�Ӧb������ת������ͬ
��������֪���ݿ��Լ��㷴Ӧb��ƽ�ⳣ��
��������֪���ݿ��Լ��㷴Ӧb�ų�������E
��ƽ��ʱa��b������Ӧ�İ����������Ϊ1:1
��3���¶�Ϊ400�桢ѹǿΪ30Mpa������£��ܱ������з��������뵪���ĺϳɰ���Ӧ��N2(g)+3H2(g)  2NH3(g)
��H��0 ��
2NH3(g)
��H��0 ��
���������ʵ���[n(NH3)]�����������ʵ���[n(H2)]��ʱ��仯�Ĺ�ϵ����ͼ��

����Ӧ�������ĵ��� ��ѡ��a��b��c��d�е�һ�����������������ʵ���[n(N2)]��ȵ������� ��ѡ��a��b��c��d�е������������������������䣬���¶ȸ�Ϊ600�棬����ͼ�л�����Ӧ�ﵽƽ��Ĺ����а����ı仯���ߡ�
��4����ҵ�ϳɰ���ú�Ʊ�ԭ��������ʱ�������ŷŴ����Ķ�����̼��ʵ�ʹ�ҵ�����п����ö�����̼�������������ѣ�CH3OCH3����һ�������£����ݻ��̶����ܱ��豸�з�����Ӧ��
2CO2(g)��6H2(g) CH3OCH3(g)��3H2O(g) ��H��0
CH3OCH3(g)��3H2O(g) ��H��0
�����ܱպ������������¶Ⱦ�ΪT�ұ��ֲ��������½���������Ӧ��һ��ʱ����������������й����ݼ����淴Ӧ���ʹ�ϵ���±���
|
���� |
c(CO2) /mol��L��1 |
c(H2) /mol��L��1 |
c(CH3OCH3) /mol��L��1 |
c(H2O) /mol��L��1 |
v (��)��v (��)�Ƚ� |
|
����I |
1.0��10��2 |
1.0��10��2 |
1.0��10��4 |
1.0��10��4 |
v (��)��v (��) |
|
����II |
2.0��10��2 |
1.0��10��2 |
1.0��10��4 |
2.0��10��4 |
|
����I�еķ�Ӧ (ѡ��ǡ���)�ﵽƽ��״̬���÷�Ӧ���¶�ΪTʱ��ƽ�ⳣ��K= �������ڵĿո�v(��)��v(��)�Ĵ�С��ϵ�� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com