
| A、NaHSO3与Na2SO3混合溶液中:3c(Na+)=c(HSO3-)+c(SO32-) |
| B、0.1 mol/L的醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后溶液显酸性:c(CH3COO-)>c(CH3COOH)>c(Cl-)>c(H+) |
| C、等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D、向1.00 L 0.3 mol/LNaOH溶液中缓慢通入0.2 mol CO2气体,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |


科目:高中化学 来源: 题型:
 已知:xA(g)+yB(g)?zC(g);△H=a.将x molA和y molB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)
已知:xA(g)+yB(g)?zC(g);△H=a.将x molA和y molB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)| A、x+y=z;a>0 |
| B、x+y>z;a<0 |
| C、x+y<z;a<0 |
| D、x+y<z;a>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 有机物 | 鉴别所用试剂 | 现象与结论 |
| A | 葡萄糖与果糖 | 钠 | 有气体放出的是葡萄糖 |
| B | 蔗糖与蛋白质 | 溴水 | 褪色的是蔗糖 |
| C | 油脂与蛋白质 | 浓硝酸 | 变蓝的是蛋白质 |
| D | 淀粉与蛋白质 | 碘水 | 变蓝的是淀粉 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X | B、Y | C、Z | D、R |
查看答案和解析>>
科目:高中化学 来源: 题型:
 石墨烯是一种由碳原子组成六角形成蜂巢晶格的平面薄膜,其结构模型见图.下列关于石墨烯的说法正确的是( )
石墨烯是一种由碳原子组成六角形成蜂巢晶格的平面薄膜,其结构模型见图.下列关于石墨烯的说法正确的是( )| A、是一种新型化合物 |
| B、与石墨互为同位素 |
| C、晶体中碳原子键全部是碳碳单键 |
| D、是一种有发展前途的导电材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(CO2)c(H2) |
| c(CO)c(H2O) |
| A、该反应的焓变为负值 | |||
| B、恒温恒容下,增大压强,H2浓度一定减小 | |||
| C、升高温度,逆反应速率减小 | |||
D、该反应的化学方程式为CO+H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
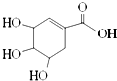
| A、分子式为C7H6O5 |
| B、分子中含有两种官能团 |
| C、可发生加成和取代反应 |
| D、在水溶液中羟基和羧基均能电离出氢离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
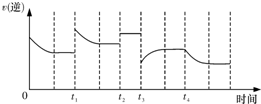 合成氨反应:N2(g)+3H2(g)?2NH3(g)△H<0.在反应过程中,逆反应速率的变化如图所示,下列说法正确的是( )
合成氨反应:N2(g)+3H2(g)?2NH3(g)△H<0.在反应过程中,逆反应速率的变化如图所示,下列说法正确的是( )| A、t1时一定是增加了生成物 |
| B、t2时使用了催化剂 |
| C、t3时增大了压强 |
| D、t4时一定是降低了温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com