
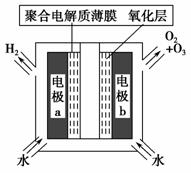
臭氧是常见的强氧化剂,广泛用于水处理系统。制取臭氧的方法很多,其中高压放电法和电解纯水法原理如下图所示,下列有关说法不正确的是 ( )。
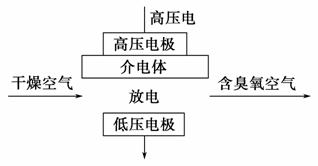
A.高压放电法,反应的原理为3O2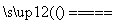 2O3
2O3
B.高压放电出来的空气中,除含臭氧外还含有氮的氧化物
C.电解时,电极b周围发生的电极反应有3H2O-6e-===O3↑+6H+和
2H2O-4e-===O2↑+4H+
D.电解时,H+由电极a经聚合固体电解质膜流向电极b
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
下列关于蛋白质的说法不正确的是 ( )
A.蛋白质是天然高分子化合物
B.通常用酒精消毒,其原理是酒精使细菌中的蛋白质变性而失去生理活性
C.浓的Na2SO4溶液能使溶液中的蛋白质析出,加水后析出的蛋白质又溶解,但已失去生理活性
D.鉴别织物成分是蚕丝还是“人造丝”可采用灼烧闻气味的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
①有化学键破坏的变化一定属于化学变化 ②发生颜色变化的一定是化学变化 ③电解的过程一定发生化学变化 ④用糯米、酒曲和水制成甜酒酿,一定是化学变化
A.①③ B.②③④ C.③④ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大。已知A与D,C与F分别同主族,D、E、F、G同周期,A分别与B、C可形成含有10个电子的共价化合物分子,B的最外层电子数是其次外层电子数的2倍,且A、B的最外层电子数之和比C的最外层电子数少1;E位于B的前一主族。
请回答下列问题。
(1)元素G在周期表中的位置为__________________,F的原子结构示意图为____________________。
(2)A、C、D三种元素组成一种常见化合物,该化合物所含的化学键类型为____________________,工业上利用某一反应可同时生产该化合物和G的单质,写出该反应的离子方程式____________________。
(3)D、E元素的最高价氧化物对应的水化物之间反应的离子方程式为___________________。
(4)含有E的简单阳离子的盐常用作净水剂,其原因为
________________________________________________________________________
(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是_________________________________________________________________
(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为________。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是______________________________________________
_______________________________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是_______________________________________________________________。
(3)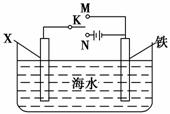 利用右图装置,可以模拟铁的电化学防护。
利用右图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于________处。若X为锌,开关K置于M处,该电化学防护法称为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于以下三个反应,从正反开始进行达到平衡后,保持温度、体积不变,按要求回答下列问题。
(1)PCl5(g)PCl3(g)+Cl2(g)
再充入PCl5(g)平衡向________方向移动,达到平衡后,PCl5(g)的转化率________,PCl5(g)的百分含量______。
(2)2HI(g)I2(g)+H2(g)
再充入HI(g)平衡向________方向移动,达到平衡后,HI的分解率________,HI的百分含量________。
(3)2NO2(g)N2O4(g)
再充入NO2(g),平衡向________方向移动,达到平衡后,NO2(g)的转化率________,NO2(g)的百分含量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响 ,实验结果如下图所示(注:T1、T2均大于300 ℃):
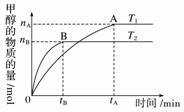
下列说法正确的是____(填序号)。
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为
v(CH3OH)=mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时增大
(4)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )
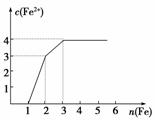
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com