
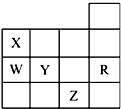
 如图为元素周期表前四周期的一部分,下列 有关R、W、X、Y、Z 5种元素的叙述中,正确的是( )
如图为元素周期表前四周期的一部分,下列 有关R、W、X、Y、Z 5种元素的叙述中,正确的是( )| A. | 常压下5种元素的单质中Z单质的沸 点最高 | |
| B. | Y、Z的阴离子电子层结构都与R原子的相同 | |
| C. | Y元素的非金属性比W元素的非金属性强 | |
| D. | W的氢化物的还原性比Y的氢化物的还原性弱 |
分析 由五种元素在周期表中的位置可知,X为N元素,W为P元素,Y为S元素,Z为Br元素,R为Ar元素,根据元素在周期表中的位置,结合元素周期律的递变规律解答该题.
解答 解:由五种元素在周期表中的位置可知,X为N元素,W为P元素,Y为S元素,Z为Br元素,R为Ar元素,则
A.常压下五种元素的单质中,P、S的单质都为固体,而Br的单质为液体,则Br单质的沸点不最高,故A错误;
B.S的阴离子电子层结构与R原子的相同,而Br的阴离子电子层结构与R原子的不相同,故B错误;
C.W为P元素,Y为S元素,位于同周期,原子序数大的非金属性强,则S的非金属性强于P,故C正确;
D.同周期元素的非金属性从左到右逐渐增强,S元素的非金属性比P元素的非金属性强,则W的氢化物的还原性比Y的氢化物的还原性弱,故D正确.
故选CD.
点评 本题考查位置、结构与性质的关系,为高频考点,把握原子结构、元素的位置与性质、元素周期律为解答的关键,综合性较强,侧重分析与应用能力的考查,题目难度不大.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 空气中:SO2、NO、N2、CO2 | |
| B. | 0.1mol•L-1的NaNO3溶液中:K+、I-、Cl-、SO42- | |
| C. | 与铝反应生成大量氢气的溶液中:Mg2+、K+、Cl-、NO3- | |
| D. | 铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上炼铁时,常用石灰石除去铁矿石中的SiO2 | |
| B. | 工业上用接触法制硫酸,在接触室里制出硫酸 | |
| C. | 工业上用二氧化硅在高温下与焦炭反应制得高纯度的硅 | |
| D. | 工业上主要从海水中提取碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑦⑧ | B. | ③④⑦⑧ | C. | ②⑤⑧⑨ | D. | ④⑦⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 钢铁在潮湿的空气中比在干燥空气中更容易生锈 | |
| B. | 用加热蒸干AlCl3溶液的方法不能制得无水AlCl3 | |
| C. | 蒸馏水和0.1 mol•L-1NaOH溶液中的c(H+),前者大于后者 | |
| D. | 已知N2(g)+3H2(g)?2NH3(g),工业上合成氨常在高压下进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑥⑦ | B. | ③④ | C. | ③④⑦ | D. | ③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com