
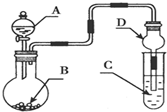
| A. | 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解 | |
| B. | 若A为浓盐酸,B为KMnO4,C中盛品红溶液,则C中溶液褪色 | |
| C. | 若A为浓H2SO4,B为Cu,C中盛有澄清石灰水,则C中溶液变浑浊 | |
| D. | 若A为浓H2SO4,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色 |
分析 A.生成的氨气与C中氯化铝反应,生成白色沉淀不能溶解;
B.浓盐酸与KMnO4反应生成氯气,氯气与水反应生成的HClO具有漂白性;
C.浓硫酸与Cu反应需要加热;
D.浓H2SO4与Na2SO3固体反应生成二氧化硫,二氧化硫为酸性氧化物.
解答 解:A.生成的氨气与C中氯化铝反应,生成白色沉淀不能溶解,则观察到C中产生白色沉淀,故A错误;
B.浓盐酸与KMnO4反应生成氯气,氯气与水反应生成的HClO具有漂白性,则C中品红溶液褪色,故B正确;
C.浓硫酸与Cu反应需要加热,不能生成二氧化硫,C中无现象,故C错误;
D.浓H2SO4与Na2SO3固体反应生成二氧化硫,二氧化硫为酸性氧化物,则C中石蕊溶液变红,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol碳正离子CH5+所含的电子数为11NA | |
| B. | 标准状况下,22.4L辛烷完全燃烧后生成二氧化碳分子数为8NA | |
| C. | 0.5mol乙烷分子中含共价键3.5NA | |
| D. | 乙烷可以发生氧化反应和取代反应.30g乙烷完全燃烧消耗3.5mol氧气,与氯气反应生成C2H4Cl2时,一定为纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的电负性呈周期性变化 | |
| B. | 元素的第一电离能呈周期性变化 | |
| C. | 元素原子的核外电子排布呈周期性变化 | |
| D. | 元素的金属性、非金属性呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L H2O含有分子数为NA | |
| B. | 分子总数为NA的N2气体体积约为22.4 L | |
| C. | 常温常压下,1.6 g CH4含分子数为0.1NA | |
| D. | 常温常压下,3.2g氧气所含氧原子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | ------- |
| V (NaOH)mL | 20.0 | 40.0 | 60.0 | 80.0 | 100.0 |
| m(沉淀)/g | 1.29 | 3.09 | 4.89 | 5.4 | 5.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据金属失去电子的多少来判断,失去电子较多的金属性较强 | |
| B. | 用钠置换MgCl2溶液中的Mg2+,来验证钠的金属性强于Mg | |
| C. | Mg不与NaOH溶液反应而Al能与NaOH溶液反应,可说明金属性:Al>Mg | |
| D. | 碱性:NaOH>Mg(OH)2>Al(OH)3,可说明钠、镁、铝金属性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 弱电解质的电离是一个吸热的过程 | |
| B. | 化学反应中的能量变化不仅仅表现为热量变化 | |
| C. | 反应物的总能量大于生成物的总能量的反应是吸热反应 | |
| D. | 断裂化学键吸收能量,形成化学键放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
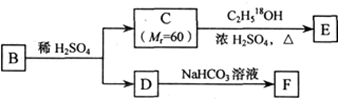
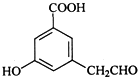 、
、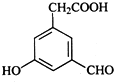 .
.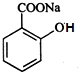 ;
;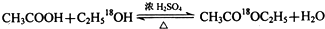 ②D与浓溴水反应
②D与浓溴水反应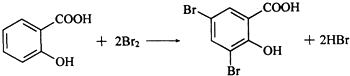
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com