
| A. | 中科院广州化学所在利用二氧化碳制取可降解塑料的技术方面处于世界领先水平,该技术的成功应用将有效改善以二氧化碳为主的温室气体引发的“厄尔尼诺”、“拉尼娜”等全球气候异常现象 | |
| B. | 许多国家对聚乙烯等塑料垃圾进行了深埋或者倾倒入海处理,达到消除“白色污染”的目的 | |
| C. | 山东单县采用以杂草、秸秆等为原料的生物质发电,有效地减少了二氧化硫的排放 | |
| D. | 汽油中掺入酒精使用,可以降低对环境的污染和节约能源 |
分析 A.利用二氧化碳制取可降解塑料可减少二氧化碳的排放;
B.深埋或者倾倒入海处理或焚烧处理,会污染土壤和空气;
C.生物质能是清洁能源;
D.乙醇汽油中乙醇属于可再生能源.
解答 解:A.利用二氧化碳制取可降解塑料可减少二氧化碳的排放,改善温室效应,故A错误;
B.对聚乙烯等塑料垃圾进行深埋或者倾倒入海处理或焚烧处理,会污染土壤和空气,故B正确;
C.生物质能是清洁能源,可减少二氧化硫的排放,故C错误;
D.乙醇汽油中乙醇属于可再生能源,所以乙醇汽油的使用可以节约能源,减少汽车尾气的污染,故D错误.
故选B.
点评 本题考查环境污染及治理,侧重于化学与人体健康的考查,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 的说法正确的是( )
的说法正确的是( )| A. | 该物质为丁烷 | B. | 该物质的分子式为C4H8 | ||
| C. | 该物质为丁烯 | D. | 该物质化学性质与苯相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
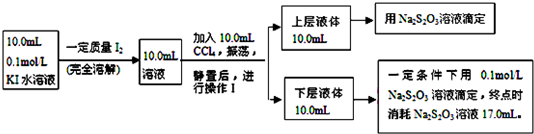
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 转移的电子数是1.204×1022 | B. | 阳极上产生112 mL O2(标准状况) | ||
| C. | 溶液的浓度变化为0.08 mol•L-1 | D. | 反应中有0.01 mol Ag被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
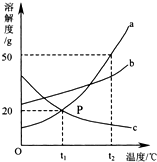 如图是A、B、C三种固体物质的溶解度曲线图,请回答:
如图是A、B、C三种固体物质的溶解度曲线图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 粒 子 | 物质的量 | 粒 子 数 | |
| H3PO4 | 0.50mol | 3.01×1023个分子 | 4 摩尔原子 |
| Na2SO4 | 0.25mol | 3.01×1023个钠离子 | 共含原子为1.75mol |
| BaCl2 | 0.5 mol | 3.01×1023 个钡离子 | 含1.0mol氯离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂与还原剂的物质的量之比为1:5 | |
| B. | 该过程说明KMnO4酸化时不能滴加盐酸 | |
| C. | 反应过程中转移2mol电子时,产生Cl2的体积约为22.4L | |
| D. | 若把该反应设计成原电池,则正极反应为MnO4-+5e-+8H+═Mn2++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 锌电极上发生还原反应 | |
| B. | 电池工作一段时间后,甲池的c(SO42-)不变 | |
| C. | 电池工作一段时间后,甲池溶液的总质量增加 | |
| D. | 该装置将化学能转化为电能,一段时间后,装置内的电子总量减少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com