
分析 (1)若铁与浓硝酸反应生成的完全为二氧化氮,根据反应C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H20、Fe+6HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Fe(NO3)3+3NO2↑+3H2O可知,当C为0时生成气体的量最少,则10g铁完全反应生成二氧化氮的物质的量为:$\frac{10g}{56g/mol}$×3≈0.536mol>0.300mol,所以铁与硝酸反应生成的气体为NO、NO2的混合物;再根据气体用50.00mL 12.00mol/L的NaOH溶液(氢氧化钠远远过量)完全吸收后,只生成两种盐可知,生成的盐为碳酸钠和亚硝酸钠,说明生成的NO、NO2的物质的量相等,设NO、NO2的物质的量都为x,该碳素钢中含有C为y,
根据反应C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H20可知,ymolC与浓硝酸反应生成ymol二氧化碳、4ymol二氧化氮,
铁与浓硝酸反应生成的二氧化氮为:x-4y,根据反应Fe+6HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Fe(NO3)3+3NO2↑+3H2O、Fe+4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$Fe(NO3)3+NO↑+2H2O可知,该钢中含有铁的物质的量为:$\frac{3}{2}$x+$\frac{1}{3}$(x-4y),根据该钢的质量可得:①[x+$\frac{1}{3}$(x-4y)]×56+12y=10.00,再根据气体的总物质的量可得:②y+2x=0.3,联立①②计算出x、y,再计算出该钢样的含碳量;
(2)根据(1)计算结果及反应C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H20、Fe+6HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Fe(NO3)3+3NO2↑+3H2O、Fe+4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$Fe(NO3)3+NO↑+2H2O计算出反应中消耗硝酸的总物质的量.
解答 解:(1)若铁与浓硝酸反应生成的完全为二氧化氮,根据反应C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H20、Fe+6HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Fe(NO3)3+3NO2↑+3H2O可知,当C为0时生成气体的量最少,则10g铁完全反应生成二氧化氮的物质的量为:$\frac{10g}{56g/mol}$×3≈0.536mol>0.300mol,所以铁与硝酸反应生成的气体为NO、NO2的混合物;再根据气体用50.00mL 12.00mol/L的NaOH溶液(氢氧化钠远远过量)完全吸收后,只生成两种盐可知,生成的盐为碳酸钠和亚硝酸钠,说明生成的NO、NO2的物质的量相等,设NO、NO2的物质的量都为x,该碳素钢中含有C为y,
根据反应C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H20可知,ymolC与浓硝酸反应生成ymol二氧化碳、4ymol二氧化氮,
铁与浓硝酸反应生成的二氧化氮为:x-4y,根据反应Fe+6HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Fe(NO3)3+3NO2↑+3H2O、Fe+4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$Fe(NO3)3+NO↑+2H2O可知,该钢中含有铁的物质的量为:$\frac{3}{2}$x+$\frac{1}{3}$(x-4y),根据该钢的质量可得:①[x+$\frac{1}{3}$(x-4y)]×56+12y=10.00,
根据气体的总物质的量可得:②y+2x=0.3,
联立①②解得:x=0.144mol、y=0.012mol,
即:该钢中含有0.012molC,其含碳量为:$\frac{12g/mol×0.012mol}{10.00g}$×100%=1.44%,
答:该钢样的含碳量为1.44%;
(2)0.012molC消耗硝酸的物质的量为:0.012mol×4=0.048mol,
生成0.144molNO消耗硝酸的物质的量为:0.144mol×4=0.576mol,
铁与浓硝酸反应生成二氧化氮的物质的量为:0.144mol-0.012mol×4=0.096mol,反应生成0.096mol二氧化氮消耗硝酸的物质的量为:0.096mol×$\frac{6}{3}$=0.192mol,
所以反应中消耗硝酸的总物质的量为:0.048mol+0.576mol+0.192mol=0.816mol,
答:参加反应的硝酸的物质的量为0.816mol.
点评 本题考查了混合物反应的计算,题目难度较大,根据生成气体的量及生成两种盐判断反应气体组成及生成固体的组成为解答关键,注意明确一氧化氮、二氧化氮与氢氧化钠溶液的反应原理,试题侧重考查学生的分析、理解能力.


科目:高中化学 来源: 题型:解答题
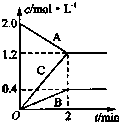 如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:
如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 1 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
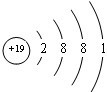 .
.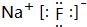 .
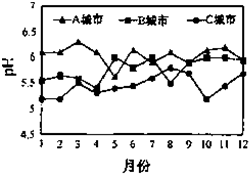
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原原理 | B. | 溶解沉淀原理 | C. | 平衡移动原理 | D. | 物质两性原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10ml0.5mol/LCH3COONa溶液与6mL1mol/L盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| B. | 0.1mol/LpH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) | |
| C. | 在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-) | |
| D. | c(NH4+)相等的(NH4)2SO4溶液,(NH4)2CO3溶液和NH4Cl溶液:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
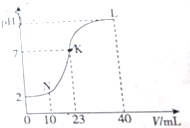
| A. | K点时的溶液:n(A-)=n(M+)=2×10-4 mol | |
| B. | N点时的溶液:2c(M+)=c(A-) | |
| C. | L点时的溶液中一定存在:c(M+)>c(A-)>c(OH-)>c(H+) | |
| D. | 水电离的程度:K>L>N |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl、NaOH | B. | CO2、HCl | C. | CaCl2、NH4NO3 | D. | Na2O2、H2O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com