
为了证明一水合氨(NH3·H2O)是弱电解质,甲、乙二人分别选用下列试剂进行实验:氨水、0.10 mol•L-1NH4Cl溶液、NH4Cl晶体、酚酞试液、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.010mol•L-1氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一方法是否正确?___________ (填“正确”或“不正确”),并说明理由_______________________;
(2)乙取出10mL 0.010mol•L-1氨水,用pH试纸测其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测其pH为b,若要确认NH3·H2O是弱电解质他认为只要a、b满足什么关系?________________;
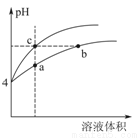
(3)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中abc三点对应的溶液中水的电离程度由大到小的顺序是 ___________;该醋酸溶液稀释过程中,下列各量一定变小的是____________。
a.c(H+) b.c(OH-) c.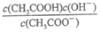 d.
d.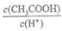
(4)在t℃时,某NaOH稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:①该温度下水的离子积常数Kw=___________(mol/L)-2;
②在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=_________。
科目:高中化学 来源:2015-2016学年黑龙江省高一上期末化学试卷(解析版) 题型:选择题
已知Fe3O4可表示成FeO·Fe2O3,水热法制备Fe3O4纳米颗粒的总反应为: 3Fe2++2S2O32-+O2 +4OH-== Fe3O4+S4O62-+2H2O。下列说法正确的是( )
A.O2和S2O32-是氧化剂,Fe2+是还原剂
B. 若有2 mol Fe2+被氧化,则被Fe2+还原的O2为0.5 mol
C. 每生成1 mol Fe3O4,转移电子的物质的量为2 mol
D. 参加反应的氧化剂与还原剂的物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一上学期12月月考化学试卷(解析版) 题型:填空题
完成下列各题
(1)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是 __(填“CaCl2”或“Ca(ClO)2”)。
(2)某些合成染发剂含有对苯二胺(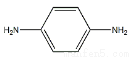 ),有一定的致癌作用。对苯二胺属
),有一定的致癌作用。对苯二胺属
于 (填“有机物”或“无机物” )。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省平度市高二上学期直升班抽考化学试卷(解析版) 题型:实验题
某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案。装置如图(夹持仪器略):
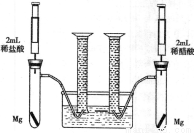
实验方案:在两试管中分别加入过量镁条,同时将两注射器中的溶液注入相应试管中,观察产生氢气的速率和体积。
(1)盐酸与镁反应的离子方程式为____________________。
(2)在上述实验方案中有一明显欠缺,该欠缺是____________。
(3)在欠缺已经得到改正的方案下,反应起始时,产生氢气的速率关系应是____________;最终产生氢气体积的关系应是_______________。
(4)实验中产生的氢气体积比理论值高,可能原因是_______________________。
(5)通过比较起始反应的速率可以得出的结论是______________。
(6)除上述方法外,还可以通过其他方向比较盐酸和醋酸的酸性,请写出其中的一种方法_________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省平度市高一上学期直升班抽考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.胶体区别于其他分散系的本质依据是具有丁达尔效应
B.通电时,溶液中的溶质粒子分别向两极移动,胶体粒子也一定会向某一极移动
C.纳米材料粒子直径一般在10-9m与10-7m之间,因此纳米材料属于胶体
D.在江河入海处容易形成沙洲与胶体的聚沉有关
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学情调查化学试卷(解析版) 题型:选择题
25℃时,水的电离可达到平衡:H2O H++OH-,下列叙述正确的是
H++OH-,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上12月月考化学试卷(解析版) 题型:推断题
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生盐和水,该反应的离子方程式为 。
(2)W与Y 可形成化合物W2Y,该化合物的电子式为 ;其水溶液中离子浓度由大到小的顺序是 。
(3)X的硝酸盐水溶液显 性,用离子方程式解释原因 。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为 。
(5)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量。写出该反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期12月月考化学试卷(解析版) 题型:选择题
某烯烃与H2加成后的产物是 , 则该烯烃的结构式可能有( )
, 则该烯烃的结构式可能有( )
A.1种 B.2种 C.3种 D.4种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北大名县一中高一上学期第二次月考化学试卷(解析版) 题型:实验题
应用下列装置,在硬质破璃管中放入还原铁粉和石棉绒的混合物加热,并通过水蒸气,就可以完成“高温下Fe与水蒸气的反应实验”。
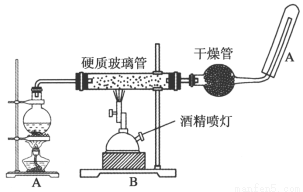
请完成该实验中的问题:
(1)写出该反应的化学方程式: ;该氧化还原反应的氧化剂是 。
(2)实验前必须对整套装置进行的操作是 。
(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是 ;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 。
(4)检验溶液中是否含有三价铁离子用 溶液(写化学式),现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com