
【题目】甲醇是重要的化工原料。在催化剂的作用下,利用合成气(主要成分为CO、CO2和H2)合成甲醇的主要化学反应如下:
I.CO+2H2![]() CH3OH II.CO2+3H2
CH3OH II.CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
Ⅲ.CO2+H2![]() CO+H2O
CO+H2O
请回答下列问题:
(1)已知三种物质的标准燃烧热如下表:
物质 | CO(g) | H2(g) | CH3OH(l) |
燃烧热(kJ·mol1) | 283.0 | 285.8 | 726.51 |
①书写25℃、101kPa条件时CO燃烧热的热化学方程式______________________。
②计算25℃、101kPa条件时反应Ⅰ的ΔH=_____kJ·mol1 。
(2)直接甲醇燃料电池(Direct Methanol Fuel Cell)属于质子交换膜燃料电池,其工作原理如图所示:
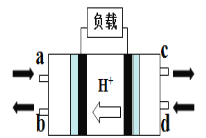
①c处产生的气体是________
②负极的电极反应式是____________。
(3)下图是甲醇燃料电池工作示意图,其中A,B,D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A,B两极上产生的气体体积相同。
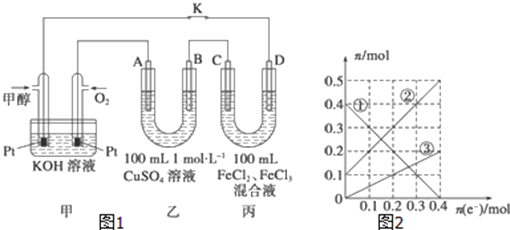
①乙中B极的电极反应式_______;
②乙中A极析出的气体在标况下的体积________;
③丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则③线表示的是____的变化,反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要____ml 5mol/L NaOH溶液。
【答案】CO (g)+![]() O2(g)= CO2(g) △H= -283.0 kJmol-1 -128.09 CO2 CH3OH+H2O-6e-=CO2↑+6H+ Cu2++2e-=Cu 2H++2e-=H2↑ 2.24L Fe2+ 280ml
O2(g)= CO2(g) △H= -283.0 kJmol-1 -128.09 CO2 CH3OH+H2O-6e-=CO2↑+6H+ Cu2++2e-=Cu 2H++2e-=H2↑ 2.24L Fe2+ 280ml
【解析】
(1)①25℃、101kPa条件时,1mol可燃物完全燃烧生成稳定氧化物放出的热量为燃烧热;
②结合燃烧热概念书写燃烧热的热化学方程式,利用盖斯定律计算得到;
(2)①甲醇燃料电池工作时,阳离子向正极移动;
②甲醇燃料电池的负极发生氧化反应,应为甲醇在负极发生氧化反应,氧化产物为CO2,并得到H+;
(3)①分析可知B电极与电源负极连接,为电解池的阴极,铜离子得电子生成铜,工作一段时间后,断开K,此时A,B两极上产生的气体体积相同说明铜离子全部放电后溶液中氢离子放电生成氢气;
②工作一段时间后,断开K,此时A、B两极上产生的气体体积相同,分析电极反应,B为阴极,溶液中铜离子获得电子变为铜单质析出,氢离子得到电子生成氢气;A电极为阳极,溶液中的氢氧根离子失电子生成氧气;阳极电极反应和电子守恒计算得到;
③C电极为阳极,D电极为阴极,根据丙图可知溶液中有三种金属阳离子,而根据丙的成分可知溶液中只有两种金属阳离子,说明在电解过程中还有Cu2+生成,因此C电极是Cu电极,作阳极,D电极是石墨作阴极,根据转移电子的物质的量和金属阳离子的物质的量的变化确定曲线对应的离子,结合转移电子的物质的量计算。
(1)①25℃、101kPa条件时CO燃烧热为-283.0kJ/mol,燃烧热的热化学方程式为;CO (g)+![]() O2(g)=CO2(g) △H= -283.0kJmol-1;
O2(g)=CO2(g) △H= -283.0kJmol-1;
②I. CO (g)+![]() O2(g)=CO2(g) △H= -283.0kJmol-1;
O2(g)=CO2(g) △H= -283.0kJmol-1;
Ⅱ.H2(g)+![]() O2(g)=H2O(l) △H=-285.8kJmol-1;
O2(g)=H2O(l) △H=-285.8kJmol-1;
Ⅲ.CH3OH(l)+![]() O2(g)=2H2O(l)+CO2(g) △H= -726.51kJmol-1;
O2(g)=2H2O(l)+CO2(g) △H= -726.51kJmol-1;
根据盖斯定律计算Ⅰ+Ⅱ×2-Ⅲ得到:CO(g)+2H2(g)![]() CH3OH(l) △H= -128.09kJ/mol;
CH3OH(l) △H= -128.09kJ/mol;
(2)①甲醇燃料电池工作时,阳离子向正极移动,由图可知c极为负极,则生成的气体为CO2;
②甲醇燃料电池的负极发生氧化反应,则甲醇在负极发生氧化反应,氧化产物为CO2,并得到H+,发生反应的电极反应式为CH3OH+H2O-6e-=CO2+6H+;
(3)①分析可知:B电极为电解池的阴极,Cu2+离子在阴极得电子生成单质Cu,电极反应为:Cu2++2e-=Cu,工作一段时间后,断开K,此时A,B两极上产生的气体体积相同,说明Cu2+全部放电后溶液中H+放电生成H2,此时电极反应为:2H++2e-=H2↑;
②工作一段时间后,断开K,此时A、B两极上产生的气体体积相同,分析电极反应,B为阴极,溶液中铜离子析出,H+放电生成H2,设生成气体物质的量为x,溶液中铜离子物质的量为n(Cu2+)=0.1L×1mol/L=0.1mol,电极反应为:Cu2++2e-=Cu,则 0.1mol Cu2+反应获得0.2mol电子,根据电极反应式:2H++2e-=H2↑可知:产生x mol H2转移2x mol电子,A电极为阳极,溶液中的氢氧根离子失电子生成氧气,电极反应为:4OH--4e-=2H2O+O2↑,产生x mol O2,失去4mol电子,根据同一闭合回路中电子转移数目相等可得0.2+2x=4x,解得x=0.1mol,乙中A极析出的气体是氧气物质的量n(O2)=0.1mol,其在标准状况下的体积V=0.1mol×22.4L/mol=2.24L;
③根据转移电子的物质的量和金属阳离子的物质的量的变化图象可知,铜离子从无逐渐增多,Fe3+物质的量减小,Fe2+增加,①为Fe3+,②为Fe2+,③为Cu2+,依据②计算得到电子转移为0.2mol,当电子转移为0.2mol时,丙中阳极电极反应Cu-2e-=Cu2+,生成Cu2+物质的量为0.1mol,图象分析每个单位为0.1mol,阴极电极反应Fe3++e-=Fe2+,溶液中有Fe3+ 0.2mol,Fe2+ 0.3mol,Cu2+为0.1mol,所以需要加入NaOH溶液1.4mol,所以NaOH溶液等体积V(NaOH)=![]() =0.28L=280mL。
=0.28L=280mL。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述正确的是
①常温下64 g S4和S8混合物中含有原子数为2NA
②2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA
③1.0L1.0mol/LCH3COOH溶液中,CH3COOH分子数为NA
④8.8g乙酸乙酯中含共用电子对数为1.4NA
⑤足量铁在1mol氯气中加热反应,铁失去的电子数为3NA
⑥常温常压下,17g甲基(-14CH3)所含的中子数为9NA
⑦标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA
⑧lmolC15H32分子中含碳碳键数目为14NA
A. ①③⑤⑦B. ①②④⑧C. ②③⑥⑧D. ①②⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组进行氯气性质的实验探究,设计了如图实验装置来制备并验证氯气的性质(部分夹持装置未画出)。请回答相关问题:
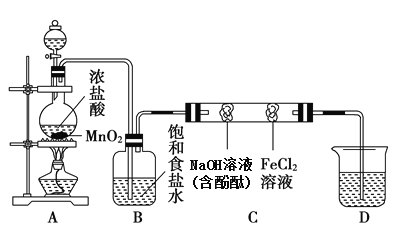
(1)A中放置固体二氧化锰的装置名称是_________。
(2)制备实验开始时,先检查装置气密性,如何检查整套装置的气密性?_____________________________________________________________。
(3)检查完装置的气密性后,接下来的操作依次是________(填序号)。
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中加入浓盐酸
(4)写出A中反应的化学方程式________________________________。
(5)装置B的作用是______________________________________________。
(6)硬质玻璃管C中事先装有两个蘸有相关试剂的棉球,左侧棉球的实验现象为________________;产生该现象的原因可能是: _______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下实验操作及现象均正确的是![]()
A. 实验Ⅰ:产生红褐色沉淀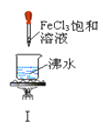
B. 实验Ⅱ:溶液颜色变红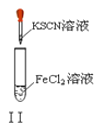
C. 实验Ⅲ:放出大量气体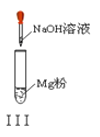
D. 实验Ⅳ:先出现白色沉淀,后溶解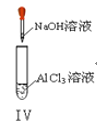
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是

A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B. 阴极区,在氢化酶作用下发生反应H2+2MV2+![]() 2H++2MV+
2H++2MV+
C. 正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D. 电池工作时质子通过交换膜由负极区向正极区移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A由C、H、O三种元素组成,相对分子质量为90。将9.0 g A 完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g。A能与NaHCO3溶液发生反应,且2分子A之间脱水可生成六元环化合物。有关A的说法正确的是
A. 分子式是C3H8O3
B. 0.1 mol A与足量Na反应产生2.24 L H2(标准状况)
C. A催化氧化的产物能发生银镜反应
D. A在一定条件下发生缩聚反应的产物是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.08g某有机物在过量纯氧中完全燃烧,可生成二氧化碳3.08g,水0.72g,同时消耗氧气2.72g。又知该有机物蒸气1.12L(已折算成标准状况下)的质量为5.4g。则
(1)求该有机物的分子式。__________________
(2)若该有机物跟FeCl3溶液作用显紫色,其一溴代物共有三种同分异构体,写出该有机物的结构简式。________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZnC2、Al4C3、Mg2C3、Li2C2等与CaC2和H2O反应相似.下列说法不正确的是( )
A. C22﹣的电子式是[![]() ]2﹣
]2﹣
B. Mg2C3和Li2C2与水反应生成的烃可能具有相同的官能团
C. 1mol ZnC2与水反应生成的烃的体积约为22.4L
D. Al4C3与水反应生成的烃分子中只有极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸银是一种无色晶体,常用于照相、制镜、印刷、医药等。其水溶液和固体常被保存在棕色试剂瓶中。硝酸银不稳定,受热分解生成固体、NO2 和 O2 。为了验证 AgNO3 受热分解的产物,某同学设计了以下实验,实验所用的装置如图(图中加热、夹持仪器等均略去):
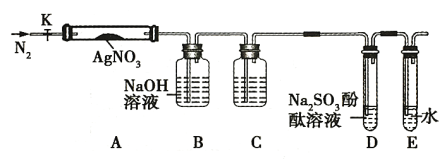
实验步骤:
a.仪器连接后,放入AgNO3固体之前,关闭K,微热硬质玻璃管A;
b.称取 AgNO3 固体1.7g 置于A中,先通一段时间N2,再关闭K,用酒精灯加热硬质玻璃管A;
c.待样品完全分解,装置A冷却至室温,称量,测得剩余固体的质量为1.08 g。
请回答下列问题:
(1)使用酒精灯对AgNO3固体加热的操作方法是_________________。
(2)步骤a的操作目的是__________________。
(3)步骤b中先通一段时间的N2的目的是_____________________。
(4)装置C瓶中盛装的药品名称为_____________(合理即可),装置D中可观察到的实验现象为__________________。
(5)根据实验现象和称量结果,请写出该装置中AgNO3固体受热分解的化学方程式__________________。
(6)从实验安全角度考虑该装置存在缺陷,应如何改进?__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com