
【题目】用2-溴丙烷制取1,2-丙二醇[(CH3CH(OH)CH2OH)]经过三步。请写出相应的化学方程式,注明反应类型。
(1)___________ 反应类型 ___________
(2)__________ 反应类型 ___________
(3)_________ 反应类型 ____________
【答案】CH3CHBrCH3+NaOH![]() CH3CH=CH2 ↑ +NaBr+ H2O 消去反应 CH2= CHCH3+ Br2→ CH2Br —CHBrCH3 加成反应 CH3CHBrCH2Br+ 2NaOH
CH3CH=CH2 ↑ +NaBr+ H2O 消去反应 CH2= CHCH3+ Br2→ CH2Br —CHBrCH3 加成反应 CH3CHBrCH2Br+ 2NaOH![]() CH3CH(OH)CH2OH+2NaBr 水解反应或取代反应
CH3CH(OH)CH2OH+2NaBr 水解反应或取代反应
【解析】
用2-溴丙烷制取1,2-丙二醇[(CH3CH(OH)CH2OH)],2-溴丙烷发生消去反应,得到的产物再发生加成,加成产物再发生水解。
⑴2-溴丙烷发生消去反应生成丙烯,反应方程式为CH3CHBrCH3+NaOH![]() CH3CH=CH2 ↑ +NaBr+ H2O;故答案为:CH3CHBrCH3+NaOH
CH3CH=CH2 ↑ +NaBr+ H2O;故答案为:CH3CHBrCH3+NaOH![]() CH3CH=CH2 ↑ +NaBr+ H2O;消去反应。
CH3CH=CH2 ↑ +NaBr+ H2O;消去反应。
⑵丙烯与溴单质发生加成反应生成CH2Br—CHBrCH3,反应方程式为CH2= CHCH3+ Br2→ CH2Br—CHBrCH3;故答案为:CH2= CHCH3+ Br2→ CH2Br—CHBrCH3;加成反应。
⑶CH2Br—CHBrCH3发生水解反应(取代反应)生成CH3CH(OH)CH2OH,反应方程式为CH3CHBrCH2Br+ 2NaOH![]() CH3CH(OH)CH2OH+2NaBr;故答案为:CH3CHBrCH2Br+ 2NaOH
CH3CH(OH)CH2OH+2NaBr;故答案为:CH3CHBrCH2Br+ 2NaOH![]() CH3CH(OH)CH2OH+2NaBr;水解反应或取代反应。
CH3CH(OH)CH2OH+2NaBr;水解反应或取代反应。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z,它们在周期表中位置如图所示,X的一种氢化物与其最高价氧化物对应水化物反应生成盐。下列说法正确的是
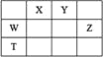
A. X的氢化物的沸点一定低于同主族元素形成的其他氢化物
B. 由Y、Z和氢三种元素形成的化合物中,Z的化合价越高氧化性越强
C. W的氧化物是酸性氧化物,能与碱、水反应,不能与酸反应
D. T元素单质具有半导体的特性,T与Y元素可形成两种化合物TY和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家认为,氢气是一种高效而无污染的理想能源,近20年来,对氢能源的研究获得了迅速发展。
(1)已知1 mol H2完全燃烧时放出285.8 kJ的热量,试写出H2燃烧的热化学方程式:_________。
(2)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是_________(填序号)。
A.电解水 B.锌和稀硫酸反应 C.光解海水
(3)某学生查阅大量资料,提出下列用水制取氢气的研究方向:
①研究在水不发生化学反应的情况下制取氢气,同时释放能量。
②设法将太阳光聚焦,产生高温,使水分解产生氢气。
③寻找高效催化剂,提高水在一定条件下分解产生氢气的转化率。
④寻找特殊化学物质,用于开发廉价能源,用以分解水制取氢气
请你从上述研究方向中,选择其中不合理的项,并简述理由:不合理的是_________,理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】法国格勒诺布尔(![]() )约瑟夫﹒傅立叶大学的研究小组发明了第一块可植入人体为人造器官提供电能的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶(蛋白质)的作用下发生反应:
)约瑟夫﹒傅立叶大学的研究小组发明了第一块可植入人体为人造器官提供电能的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶(蛋白质)的作用下发生反应:![]() (酸性环境)。下列有关该电池的说法不正确的是( )
(酸性环境)。下列有关该电池的说法不正确的是( )
A.该生物燃料电池不能在高温下工作
B.该电池负极的电极反应式为![]()
C.消耗1mol氧气时转移4mol电子,![]() 向负极移动
向负极移动
D.提高葡萄糖生物燃料电池的效率,可能使其在将来可以为任何可植入医疗设备提供电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应![]() ,某研究小组将4moX和2molY置于一容积不变的密闭容器中,测定1min内X的转化率,得到的数据如表所示,下列判断正确的是( )
,某研究小组将4moX和2molY置于一容积不变的密闭容器中,测定1min内X的转化率,得到的数据如表所示,下列判断正确的是( )
t/min | 2 | 4.5 | 5 | 6 |
X的转化率 | 30% | 40% | 70% | 70% |
A.随着反应的进行,混合气体的密度不断增大
B.反应在5.5min时,![]()
C.6min时,容器中剩余1.4molY
D.其他条件不变,将X的物质的量改为10mol,则可得到4molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下所示。下列说法错误的是

A.甲位于现行元素周期表第四周期第ⅢA族
B.原子半径比较:甲>乙>Si
C.原子序数:甲-Ca=1
D.推测乙的单质可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验事实的解释正确的是( )
现象 | 解释或结论 | |
A | SO2使酸性高锰酸钾溶液褪色 | SO2表现漂白性 |
B | 向某溶液中加入BaCl2溶液和稀HNO3,若有白色沉淀生成 | 原溶液中含SO42- |
C | 用铂丝蘸取某溶液在酒精灯火焰上灼烧直接观察火焰颜色,未见紫色 | 原溶液中不含K+ |
D | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的强 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
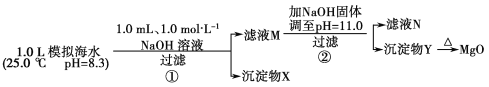
模拟海水中的离子浓度/mol·L-1 | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10-5 mol·L-1,可认为该离子不存在;实验过程中,假设溶液体积不变。Ksp[CaCO3]=4.96×10-9,Ksp[MgCO3]=6.82×10-6,Ksp[Ca(OH)2]=4.68×10-6,Ksp[Mg(OH)2]=5.61×10-12。下列说法正确的是( )
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列说法中正确的是( )
A.1mol苯乙烯![]()
![]()
![]() 中含有的C=C数为4NA
中含有的C=C数为4NA
B.2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2 NA
C.0.1molCnH2n+2中含有的C—C键数为0.1nNA
D.标准状况下,2.24LCHCl3含有的分子数为0.1 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com