
【题目】富铁铝土矿(主要含有Al2O3、Fe2O3、FeO和SiO2)可用于制备净水剂明矾KAl(SO4)212H2O和补血剂FeSO47H2O.工艺流程如下(部分操作和产物略去): 
(1)操作1的名称是 .
(2)反应①②③④中是氧化还原反应的是(填写编号).
(3)综合考虑,金属X最好选择的试剂是 , 写出该反应离子方方程式 .
(4)反应①的离子方程式是、 .
(5)溶液D中含有的金属阳离子是 , 检验方法是 .
(6)用含铝元素27%的上述矿石10吨,通过上述流程最多生产明矾吨.
【答案】
(1)过滤
(2)④
(3)Fe;Fe+2Fe3+=3Fe2+
(4)SiO2+2OH﹣=SiO32﹣+H2O;Al2O3+2OH﹣=2AlO2﹣+H2O
(5)Fe2+;检验亚铁离子的方法为:取少量溶液D于试管中,滴入硫氰化钾溶液,无现象;再滴入几滴氯水,若变红;证明含有Fe2+
(6)47.4
【解析】解:(1)经过操作1得到溶液和滤渣,分离固液的操作为过滤;所以答案是:过滤;(2)反应①②③均为复分解反应,反应④为铁还原铁离子的反应;所以答案是:④;(3)溶液B中含有Fe2(SO4)3、FeSO4及未反应的硫酸等,加入足量X后冷却、结晶、过滤得到FeSO47H2O,则X为Fe,将Fe3+转化为Fe2+ , 反应为:Fe+2Fe3+=3Fe2+;所以答案是:Fe;Fe+2Fe3+=3Fe2+;(4)反应①为富铁铝土矿中用氢氧化钾溶液溶解,氧化铝、二氧化硅反应溶解生成偏铝酸钠、硅酸钠,离子方程式为:SiO2+2OH﹣=SiO32﹣+H2O;Al2O3+2OH﹣=2AlO2﹣+H2O;所以答案是:SiO2+2OH﹣=SiO32﹣+H2O;Al2O3+2OH﹣=2AlO2﹣+H2O;(5)根据分析溶液D的金属阳离子为Fe2+;检验亚铁离子的方法为:取少量溶液D于试管中,滴入硫氰化钾溶液,无现象;再滴入几滴氯水,若变红;证明含有Fe2+;所以答案是:Fe2+;检验亚铁离子的方法为:取少量溶液D于试管中,滴入硫氰化钾溶液,无现象;再滴入几滴氯水,若变红;证明含有Fe2+;(6)用含铝元素27%的上述矿石10吨,设通过上述流程最多生产明矾质量为x,则有 ![]() =27%×10t,解得x=47.4t; 所以答案是:47.4.
=27%×10t,解得x=47.4t; 所以答案是:47.4.


科目:高中化学 来源: 题型:
【题目】某固体化合物的化学式NH5 , 它的所有原子的最外层都符合稀有气体原子的电子层结构,则下列说法中,正确的是( )
A.它与足量的水反应的化学方程式为:NH5+H2O═NH3H2O+H2↑
B.NH5中只有极性共价键的共价化合物
C.1molNH5中含有5NA个N﹣H键(NA表示阿伏伽德罗常数)
D.NH5中所有原子最外层均为8个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是 ( )
A. 18O原子核内的中子数为8 B. 16O2和18O2的化学性质几乎相同
C. H216O与H218O质子数不同 D. H2和D2 属于同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了验证SO2的性质,某同学利用输液管设计了如图1微型实验: 
回答下列问题:
(1)仪器A的名称是 .
(2)装置l中的现象是;装置3中证明SO2具有性.
(3)下列说法正确的是 .
A.装置2中紫色石蕊试液变红的原因是SO2+H2O=H2SO3 , H2SO3显酸性
B.实验结束后将输液管1加热溶液不变色
C.实验结束后,可由a导管向装置中加水,将气体赶出后再拆装置,防止残留的SO2有毒气体污染环境
D.在a导管处用向下排空气法收集SO2
(4)装置4中酸性高锰酸钾褪色,经测定反应后溶液中含有Mn2+和SO42﹣ , 请写出该反应的离子方程式 .
(5)该学生还利用上图部分仪器组装成的装置(如图2)证明S、C、Si非金属性强弱.可共选择的试剂有:硫酸、亚硫酸、硝酸、木炭、硅酸钠溶液. 
①装置A中试剂X是;装置1中反应的化学方程式是 .
②实验结论:因为酸性强弱是>>(填化学式),故非金属性是S>C>Si.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积固定的密闭容器中,某化学反应2A(g) ![]() B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
实验 序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内,用A表示表示该反应的平均速率
为_______ mol/(L . min)
(2)在实验2,A的初始浓度c2=________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_______________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3_______v1(填>、=、<),c3=________mol/L
(4)比较实验4和实验1,可推测该反应是________反应(选填吸热、放热)。
理由是___________________________________________________________
(5)根据以上实验请指出要加快该反应可采取什么样的方法(列举方法最少2种)
________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
I.取样、氧的固定 .
用溶解氧瓶采集水样,记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
在碘量瓶中将固氧后的水样酸化,MnO(OH)2被I-还原为Mn2+(该反应放热),在暗处静置5min,然后用标准Na2S3O3溶液滴定生成的I2(2S2O32-+I2=2I- +S4O62-)。
回答下列问题:
(1)“氧的固定”中发生反应的化学方程式为___________。
(2)水样酸化后发生反应的离子方程式___________。
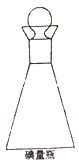
(3)在碘量瓶(如图)中进行反应,要盖上塞子且在塞子上倒少量水,这样做的目的是___________。
(4)Na2S3O3溶液不稳定,易被氕化,且易受到水中CO2以及微生物的影响而分解,配制该溶液时需要的蒸馏水必须经过煮沸冷却后才能使用,其目的是__________。
(5) Na2S3O3溶液不稳定,使用前需标定,KIO3做基准物标定Na2S3O3溶液的浓度,称取0.214g KIO3与过量的KI作用,析出的碘用Na2S3O3溶液滴定,用去24.00mL,此Na2S3O3溶液的浓度为______(已知M(KIO3) = 214.0g/mol)
(6)取100.00mL水样经固氧、酸化后,用该Na2S3O3溶液滴定,以淀粉溶液作指示剂,终点现象为_____;若消耗Na2S3O3的体积为l0mL,则水样中溶解氧的含量为______mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于硝酸的认识,不正确的是
A. 浓硝酸和稀硝酸都具有氧化性
B. 铜与硝酸的反应属于置换反应
C. 浓硝酸在常温下见光或受热会分解
D. 常温下可用铁或铝制品盛装浓硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com