
”¾ĢāÄæ”æ£ØĢāĪÄ£©Ä³ĪĀ¶ČĻĀ£¬ŌŚ2LČŻĘ÷ÖŠ3ÖÖĪļÖŹ¼ä½ųŠŠ·“Ó¦£¬ X”¢Y”¢ZµÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆĒśĻßČēĶ¼”£·“Ó¦ŌŚ t1min Ź±µ½“ļĘ½ŗā£¬ČēĶ¼ĖłŹ¾£ŗ
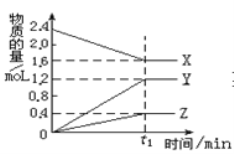
¢Å¢ŁøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ____________”£
¢ŚøĆ·“Ó¦µÄĘ½ŗā³£ŹżŹĒ___________”£
¢Ū ŌŚt1minŹ±£¬øĆ·“Ó¦“ļµ½ĮĖ__________דĢ¬£¬ĻĀĮŠæÉ×÷ĪŖÅŠ¶Ļ·“Ó¦ŅŃ“ļµ½øĆדĢ¬µÄŹĒ________£ØĢīŠņŗÅ£©”£
A£®X”¢Y”¢ZµÄ·“Ó¦ĖŁĀŹĻąµČ B£®X”¢YµÄĪļÖŹµÄĮæÅØ¶Č²»ŌŁøıä
C£®Éś³É 3mol Y µÄĶ¬Ź±Éś³É 1mol Z D£®Éś³É 1mol Z µÄĶ¬Ź±Éś³É 2mol X
¢Ę ¢ŁČōÉĻŹö·“Ó¦ÖŠX”¢Y”¢Z·Ö±šĪŖ NH3 ”¢H2 ”¢N2 £¬ĒŅŅŃÖŖ1mol°±Ęų·Ö½ā³ÉµŖĘųŗĶĒāĘųŅŖĪüŹÕ46 kJµÄČČĮ棬ŌņÓÉH2”¢N2 ŗĻ³ÉNH3 ·“Ó¦µÄČČ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗ____________________”£
¢Ś¼×”¢ŅŅĮ½Ī»Ķ¬Ń§ĢÖĀŪ·ÅČČ·“Ó¦ŗĶĪüČČ·“Ó¦£ŗ¼×Ėµ¼ÓČČŗó²ÅÄÜ·¢ÉśµÄ»Æѧ·“Ó¦ŹĒĪüČČ·“Ó¦£»ŅŅĖµ·“Ó¦ÖŠŅŖ³ÖŠų¼ÓČČ²ÅÄܽųŠŠµÄ·“Ó¦ŹĒĪüČČ·“Ó¦”£ÄćČĻĪŖĖūĆĒĖµ·ØÕżČ·µÄŹĒ__________Ķ¬Ń§”£
”¾“š°ø”æ2X![]() 3Y+Z0.0675Ę½ŗāBDN2(g)+3H2(g)
3Y+Z0.0675Ę½ŗāBDN2(g)+3H2(g) ![]() 2NH3(g) ”÷H= -92kJ / molŅŅ
2NH3(g) ”÷H= -92kJ / molŅŅ
”¾½āĪö”æ
£Ø1£©¢Łøł¾ŻĶ¼Ļń£¬XĪŖ·“Ó¦Īļ£¬YŗĶZĪŖÉś³ÉĪļ£¬øł¾Ż»Æѧ¼ĘĮæŹżÖ®±ČµČÓŚĪļÖŹµÄĮæ±ä»ÆÖ®±Č£¬Ņņ“ĖøĆ·“Ó¦·½³ĢŹ½ĪŖ2X![]() 3Y£«Z£»¢Ś“ļµ½Ę½ŗāŹ±c(X)=1.6/2mol”¤L£1=0.8mol”¤L£1£¬c(Y)=1.2/2mol”¤L£1=0.6mol”¤L£1£¬c(Z)=0.4/2mol”¤L£1=0.2mol”¤L£1£¬øł¾ŻĘ½ŗā³£ŹżµÄ±ķ“ļŹ½£¬K=0.2”Į0.63/0.82=0.0675£»¢Ūøł¾ŻĶ¼Ļń£¬ŌŚt1Ź±æĢ·“Ó¦“ļµ½Ę½ŗā£»A”¢Ć»ÓŠÖøĆ÷·“Ó¦ĖŁĀŹµÄ·½Ļņ£¬¹ŹA“ķĪó£»B”¢øł¾Ż»ÆŃ§Ę½ŗāדĢ¬µÄ¶ØŅ壬¹ŹBÕżČ·£»C”¢·“Ó¦¶¼ŹĒĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬Ņņ“Ė²»ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗā£¬¹ŹC“ķĪó£»D”¢Éś³É1molZ£¬ĖµĆ÷·“Ó¦ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬Éś³É2molX£¬ĖµĆ÷·“Ó¦ĻņÄę·“Ó¦·½Ļņ½ųŠŠ£¬ĒŅÉś³ÉĮæ±ČÖµµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬Ņņ“ĖÄܹ»ĖµĆ÷·“Ó¦“ļµ½Ę½ŗā£¬¹ŹDÕżČ·£»
3Y£«Z£»¢Ś“ļµ½Ę½ŗāŹ±c(X)=1.6/2mol”¤L£1=0.8mol”¤L£1£¬c(Y)=1.2/2mol”¤L£1=0.6mol”¤L£1£¬c(Z)=0.4/2mol”¤L£1=0.2mol”¤L£1£¬øł¾ŻĘ½ŗā³£ŹżµÄ±ķ“ļŹ½£¬K=0.2”Į0.63/0.82=0.0675£»¢Ūøł¾ŻĶ¼Ļń£¬ŌŚt1Ź±æĢ·“Ó¦“ļµ½Ę½ŗā£»A”¢Ć»ÓŠÖøĆ÷·“Ó¦ĖŁĀŹµÄ·½Ļņ£¬¹ŹA“ķĪó£»B”¢øł¾Ż»ÆŃ§Ę½ŗāדĢ¬µÄ¶ØŅ壬¹ŹBÕżČ·£»C”¢·“Ó¦¶¼ŹĒĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬Ņņ“Ė²»ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗā£¬¹ŹC“ķĪó£»D”¢Éś³É1molZ£¬ĖµĆ÷·“Ó¦ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬Éś³É2molX£¬ĖµĆ÷·“Ó¦ĻņÄę·“Ó¦·½Ļņ½ųŠŠ£¬ĒŅÉś³ÉĮæ±ČÖµµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬Ņņ“ĖÄܹ»ĖµĆ÷·“Ó¦“ļµ½Ę½ŗā£¬¹ŹDÕżČ·£»
£Ø2£©¢ŁŗĻ³É°±ŹōÓŚ·ÅČČ·“Ó¦£¬Éś³É2molNH3Ź±·Å³öµÄČČĮæĪŖ2”Į46kJ=92kJ£¬¼“ŗĻ³É°±µÄČČ»Æѧ·“Ó¦·½³ĢŹ½ĪŖN2(g)£«3H2(g)![]() 2NH3(g) ”÷H=£92kJ”¤mol£1£»¢ŚÓŠŠ©·ÅČČ·“Ó¦Ņ²ŠčŅŖ¼ÓČČ£¬ČēĀĮČČ·“Ó¦£¬Ņņ“Ė¼×Ķ¬Ń§Ėµ·Ø“ķĪó£¬ĪüČČ·“Ó¦ŹĒ³ÖŠų¼ÓČČ²ÅÄܽųŠŠ£¬¹ŹŅŅĶ¬Ń§Ėµ·ØÕżČ·”£
2NH3(g) ”÷H=£92kJ”¤mol£1£»¢ŚÓŠŠ©·ÅČČ·“Ó¦Ņ²ŠčŅŖ¼ÓČČ£¬ČēĀĮČČ·“Ó¦£¬Ņņ“Ė¼×Ķ¬Ń§Ėµ·Ø“ķĪó£¬ĪüČČ·“Ó¦ŹĒ³ÖŠų¼ÓČČ²ÅÄܽųŠŠ£¬¹ŹŅŅĶ¬Ń§Ėµ·ØÕżČ·”£


 Š”ѧ¶į¹ŚAB¾ķĻµĮŠ“š°ø
Š”ѧ¶į¹ŚAB¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀ£¬ĻĀĮŠŃ”ĻīĖłŹ¾ĪļÖŹ¼ä×Ŗ»Æ¾łÄÜŅ»²½ŹµĻֵďĒ( )
A.Cl2”śHCl”śNaClOB.Al”śNaAlO2”śAl(OH)3
C.Cu”śCuO”śCu(OH)2D.Fe”śFe(OH)3”śFeCl3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ
¢ŁH2(g)£«![]() O2(g)
O2(g) ![]() H2O(g)£»¦¤H1£½ a kJ”¤mol-1
H2O(g)£»¦¤H1£½ a kJ”¤mol-1
¢Ś2H2(g)£«O2(g) ![]() 2H2O(g)£»¦¤H2£½ b kJ”¤mol-1
2H2O(g)£»¦¤H2£½ b kJ”¤mol-1
¢ŪH2(g)£«![]() O2(g)
O2(g)![]() H2O(l)£»¦¤H3£½ c kJ”¤mol-1
H2O(l)£»¦¤H3£½ c kJ”¤mol-1
¢Ü2H2(g)£«O2(g)![]() 2H2O(l)£»¦¤H4£½ d kJ”¤mol-1
2H2O(l)£»¦¤H4£½ d kJ”¤mol-1
ĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ(””””)
A. c<a <0 B. b>a > 0 C. 2a=d <0 D. 2c=d >0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌÓŚ·“Ó¦2X(g) £« Y(g) ![]() 3Z(g)£¬ŌŚĘäĖūĢõ¼ž²»±äŹ±£¬øıäĘäÖŠŅ»øöĢõ¼ž£¬ŌņÉś³ÉZµÄĖŁĀŹ(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±)£ŗ
3Z(g)£¬ŌŚĘäĖūĢõ¼ž²»±äŹ±£¬øıäĘäÖŠŅ»øöĢõ¼ž£¬ŌņÉś³ÉZµÄĖŁĀŹ(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±)£ŗ
£Ø1£©ÉżøßĪĀ¶Č£ŗ____________£»
£Ø2£©Ōö“óŃ¹Ēæ£ŗ____________£»
£Ø3£©Ōö“óČŻĘ÷ČŻ»ż£ŗ______________£»
£Ø4£©¼ÓČė X £ŗ______________£»
£Ø5£©¼ÓČė Y £ŗ______________£»
£Ø6£©Ń¹ĖõĢå»ż£ŗ______________£»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫“æŠæʬŗĶ“æĶʬ°“Ķ¼Ź¾·½Ź½²åČėĶ¬ÅØ¶ČµÄĻ”ĮņĖįÖŠŅ»¶ĪŹ±¼ä£¬ŅŌĻĀŠšŹöÕżČ·µÄŹĒ£Ø £©
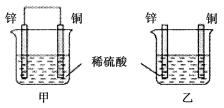
¢ŁĮ½ÉÕ±ÖŠĶʬ±ķĆę¾łĪŽĘųÅŻ²śÉś
¢Ś¼×ÖŠĶʬŹĒÕż¼«£¬ŅŅÖŠĶʬŹĒøŗ¼«
¢ŪĮ½ÉÕ±ÖŠČÜŅŗµÄc(H£«)¾ł¼õŠ”
¢Ü²śÉśĘųÅŻµÄĖŁĀŹ¼×±ČŅŅĀż
¢Ż¼×ÖŠSO42-ĻņZnʬŅĘ¶Æ£¬H£«ĻņCuʬŅʶÆ
¢ŽŅŅÖŠµēĮ÷“ÓCuʬĮ÷ĻņZnʬ
¢ß¼×ŅŅĮ½ÉÕ±ÖŠCuʬµÄÖŹĮæ¾ł²»±ä
A. ¢Ł¢Ś¢ŪB. ¢Ū¢Ż¢ß
C. ¢Ü¢Ż¢ŽD. ¢Ś¢Ū¢Ü¢Ż¢ß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æFe@Fe2O3ÄÉĆ×ĻߏĒŅ»ÖÖŠĀŠĶĢś»ł²ÄĮĻ£¬ŌŚ“߻Ɣ¢ÉśĪļŅ½Ņ©”¢»·¾³æĘѧµČĮģÓņ¾ßÓŠ¹ćĄ«Ó¦ÓĆĒ°¾°”£Ä³ŃŠ¾æŠ”×éŅŌ³ąÄą£ØĀĮĶĮæóĢįČ”Ńõ»ÆĀĮ¹ż³ĢÖŠ²śÉśµÄ¹ĢĢå·ĻĘśĪļ£¬ŗ¬SiO2”¢Fe2O3”¢Al2O3£©ĪŖŌĮĻ£¬Éč¼ĘĻĀĮŠĮ÷³ĢÖʱøFe@Fe2O3ÄÉĆ×Ļß²¢Ģ½¾æĘäŌŚĖ®“¦ĄķÖŠµÄÓ¦ÓĆ”£
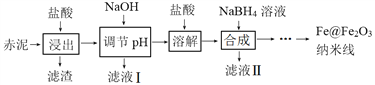
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©”°½ž³ö”±ŹµŃéÖŠ£¬ŃĪĖįĘšŹ¼ÅØ¶Č¶ŌĢś”¢ĀĮ½ž³öĀŹµÄÓ°ĻģČēĶ¼ĖłŹ¾£ŗ
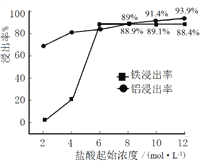
¢ŁŃĪĖįµÄŗĻŹŹÅضČĪŖ______________”£
¢ŚŃĪĖįĘšŹ¼ÅضČĪŖ2 mol”¤L©1Ź±£¬ĢśµÄ½ž³öĀŹŗܵĶ£¬ŌŅņŹĒ______________”£
£Ø2£©ŅŃÖŖ£ŗ25”ꏱ£¬Al(OH)3(s)![]() AlO2£+ H+ + H2O K=4”Į10£13”£Čō½ž³öŅŗc(Al3+) = 0.04 mol”¤L£1£¬”°µ÷½ŚpH”±Ź±£¬pH×īŠ”Ó¦ĪŖ______________£ØÉčµ÷½ŚpH¹ż³ĢÖŠČÜŅŗĢå»ż²»±ä£©”£
AlO2£+ H+ + H2O K=4”Į10£13”£Čō½ž³öŅŗc(Al3+) = 0.04 mol”¤L£1£¬”°µ÷½ŚpH”±Ź±£¬pH×īŠ”Ó¦ĪŖ______________£ØÉčµ÷½ŚpH¹ż³ĢÖŠČÜŅŗĢå»ż²»±ä£©”£
£Ø3£©Fe@Fe2O3ÄÉĆ×ĻßĪŖæĒ²ć½į¹¹£ØŗĖŹĒFe”¢æĒŹĒFe2O3£©£¬æĒŹĒÓÉÖŠŠÄĢśŗĖŌŚŗĻ³É¹ż³ĢÖŠ±»Ńõ»Æ¶ųŠĪ³É”£
¢Ł”°ŗĻ³É”±Ź±µĪ¼ÓNaBH4ČÜŅŗ¹ż³ĢÖŠ°éÓŠĘųÅŻ²śÉś£¬ĀĖŅŗ¢ņÖŠŗ¬B(OH)3£¬ŗĻ³ÉĢśŗĖµÄĄė×Ó·½³ĢŹ½ĪŖ____________________________”£
¢Ś”°ŗĻ³É”±ŗ󣬾¹żĀĖ”¢______________”¢______________»ńµĆFe@Fe2O3ÄÉĆ×Ļß”£
£Ø4£©Fe@Fe2O3ÄÉĆ×ĻßČ„³żĖ®ĢåÖŠCr2O72£µÄ»śĄķŹĒ£¬ÄÉĆ×Ļß½«Cr2O72£Īüø½ŌŚ±ķĆę²¢»¹Ō”£ŌŚ”°ĪŽŃõ”±ŗĶ”°ÓŠŃõ”±Ģõ¼žĻĀ½«ÄÉĆ×Ļß·Ö±šÖĆÓŚĮ½·ŻĻąĶ¬µÄĖ®ĢåÖŠ£¬80 minŗó»ŲŹÕøĆÄÉĆ×Ļߣ¬²āµĆĘä±ķĆęŌŖĖŲµÄŌ×ÓøöŹż±ČČēĻĀ±ķ£ŗ

¢ŁŌŚĖ®ĢåÖŠFe@Fe2O3ÄÉĆ×ĻߊĪ³ÉµÄ·ÖÉ¢ĻµŹĒ____________________________”£
¢ŚŃł±¾2µÄŹµŃéĢõ¼žŹĒ______________£ØĢī”°ÓŠŃõ”±»ņ”°ĪŽŃõ”±£©”£
¢ŪŅŃÖŖĖ®ĢåÖŠ¼ģ²ā²»µ½Cr(¢ó)£¬Ńł±¾1ÖŠFe@Fe2O3ÄÉĆ×ĻߵıķĆęCr(¢ö)µÄČ„³żĀŹĪŖ____________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ»śĪļµÄ½į¹¹æÉÓĆ”°¼üĻߏ½”±±ķŹ¾£¬ČēCH3”ŖCH£½CH”ŖCH3æɼņŠ“ĪŖ![]() £¬ÓŠ»śĪļXµÄ¼üĻߏ½ĪŖ
£¬ÓŠ»śĪļXµÄ¼üĻߏ½ĪŖ![]() ”£ĻĀĮŠ¹ŲÓŚÓŠ»śĪļXµÄĖµ·ØÖŠÕżČ·µÄŹĒ
”£ĻĀĮŠ¹ŲÓŚÓŠ»śĪļXµÄĖµ·ØÖŠÕżČ·µÄŹĒ
A. XµÄŗ¬Ńõ¹ŁÄÜĶÅŹĒōČ»łŗĶĆŃ¼ü
B. XµÄ·Ö×ÓŹ½ĪŖC7H7O3
C. XŅņÄÜÓėĖįŠŌKMnO4ČÜŅŗ·¢ÉśČ”“ś·“Ó¦¶ųĶŹÉ«
D. ÓŠ»śĪļYŹĒXµÄĶ¬·ÖŅģ¹¹Ģ壬ÄÜÓėĢ¼ĖįĒāÄĘČÜŅŗ·“Ó¦ĒŅŗ¬±½»·£¬ŌņYµÄ½į¹¹ÓŠ3ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖęŌ×ÓŠņŹżµŻŌö£¬°ĖÖÖ¶ĢÖÜĘŚŌŖĖŲ(ÓĆ×ÖÄøxµČ±ķŹ¾)Ō×Ó°ė¾¶µÄĻą¶Ō“óŠ””¢×īøßÕż¼Ū»ņ×īµĶøŗ¼ŪµÄ±ä»ÆČēĶ¼ĖłŹ¾”£
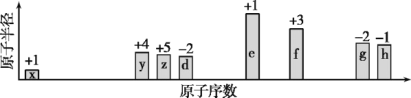
øł¾ŻÅŠ¶Ļ³öµÄŌŖĖŲ»Ų“šĪŹĢā£ŗ
£Ø1£©hŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ_______”£
£Ø2£©±Č½Ļd”¢fĄė×Ó°ė¾¶“󊔣ØÓĆ»ÆѧŹ½±ķŹ¾£¬ĻĀĶ¬£©£ŗ_>_”£g”¢hµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌĒæČõ£ŗ__ >__”£
£Ø3£©hµÄµ„ÖŹÓėeµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijČĖÉč¼Ęµķ·ŪĄūÓĆ·½°øČēĻĀĶ¼ĖłŹ¾£ŗ
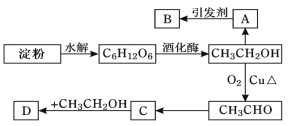
ĘäÖŠ£ŗAŹĒŅŅĻ©£¬ÄܓߏģĖ®¹ū£¬BŹĒøß·Ö×Ó»ÆŗĻĪļ£¬DŹĒÓŠĖ®¹ūĻćĪ¶µÄĪļÖŹ”£Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ
(1)”°C6H12O6”±µÄĆū³ĘŹĒ________£¬AµÄµē×ÓŹ½ĪŖ________£¬CÖŠŗ¬ÓŠ¹ŁÄÜĶÅĆū³Ę_______”£
(2) A”śB·“Ó¦ĄąŠĶ______________”£
(3)Š“³öĻĀĮŠ×Ŗ»ÆµÄ»Æѧ·½³ĢŹ½
C”śD£ŗ_____________________£¬
CH3CH2OH”śCH3CHO£ŗ_____________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com