
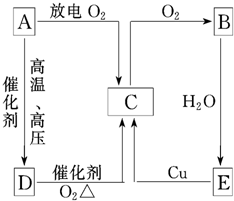
 如图表示A、B、C、D、E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色,写出A、B、D、E的化学式和有关反应的化学方程式.
如图表示A、B、C、D、E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色,写出A、B、D、E的化学式和有关反应的化学方程式.
| ||
| ||
| △ |
| ||
| △ |


科目:高中化学 来源: 题型:
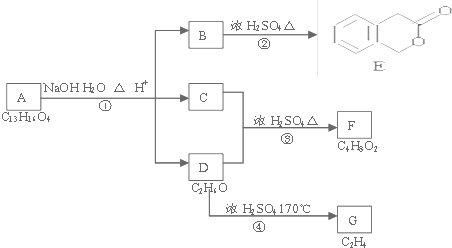
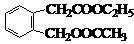
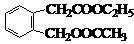
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
| 催化剂 |
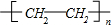 (或CH2=CH2+H2O
(或CH2=CH2+H2O| 催化剂 |
| 催化剂 |
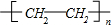 (或CH2=CH2+H2O
(或CH2=CH2+H2O| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2013?中山一模)根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
(2013?中山一模)根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| 3 |
| 4 |
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
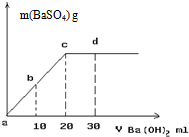 (1)服用含碘化钾的碘药片可抗核辐射.将碘片剥去糖衣皮研粹后置于试管中制得无色水溶液,并加入几滴淀粉试液,然后向试管中逐滴加入氯水,观察到溶液由无色变为蓝色,若继续滴加氯水后蓝色溶液又褪为无色,试回答下列问题:
(1)服用含碘化钾的碘药片可抗核辐射.将碘片剥去糖衣皮研粹后置于试管中制得无色水溶液,并加入几滴淀粉试液,然后向试管中逐滴加入氯水,观察到溶液由无色变为蓝色,若继续滴加氯水后蓝色溶液又褪为无色,试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com