
| 编号 | 实验 | 操作 |
| A | 钠与水的反应 | 用镊子从煤油中取出金属钠,切下绿豆大小,放入装满水的烧杯中 |
| B | 配制一定浓度的氯化钾溶液500mL | 准确称取氯化钾固体,放入到500mL的容量瓶中,加水溶解、振荡、摇匀、定容 |
| C | 闻氯气的方法 | 用手轻轻地在瓶口扇动,使极少量氯气飘进鼻孔 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个烧杯,上层液体继续从分液漏斗下端管口放出 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.放入装满水的烧杯,溶液易溅出发生危险;
B.溶解氯化钾不能放在容量瓶中;
C.闻气体气味时需避免中毒;
D.分液漏斗上层液体应该从分液漏斗的上口倒出.
解答 解:A.用镊子从煤油中取出金属钠,切下绿豆大小的钠,用滤纸擦净后小心放入装少量水的烧杯中,观察现象,故A错误;
B.配制一定物质的量浓度的溶液时,溶解在烧杯中溶解溶质,不能用容量瓶溶解,故B错误;
C.闻氯气的方法为:用手轻轻地在瓶口扇动,使极少量氯气飘进鼻孔,以避免中毒,故C正确;
D.为了避免污染试剂,下层液体从分液漏斗下端管口放出,关闭活塞,换一个烧杯,上层液体从分液漏斗上口倒出,故D错误;
故选C.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及溶液配制、分液、闻气体操作方法等知识,明确常见化学实验基本操作方法即可解答,试题侧重基础知识的考查,有利于提高学生的分析能力及化学实验能力.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下,氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) | |
| B. | 常温下,在pH=11的溶液中,水电离出的c(OH-)一定等于10-3mol/L | |
| C. | 若强酸、强碱中和后溶液的pH=7,则中和之前酸、碱的pH之和一定等于14 | |
| D. | 将物质的量浓度和体积都相同的一元酸HA与一元碱BOH混合后,溶液呈中性,则反应后溶液中c(H+)=$\sqrt{Kw}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
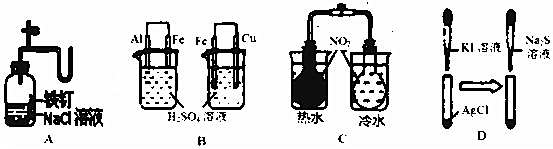
| 实验 | 实验现象 | 结论 |
| A | 广口瓶中光亮的铁钉放置一段时间后生锈 | 铁钉发生析氢腐蚀 |
| B | 左烧杯铁表面冒气泡,右烧杯铜表面冒气泡 | 金属活动性:Al>Fe>Cu |
| C | 左烧杯气体颜色加深,右烧杯气体颜色变浅 | 2NO2(g)?N2O4(g)△H>0 |
| D | 白色固体先变为黄色,后变为黑色 | Ksp:AgCl<AgI<Ag2S |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用溴的四氯化碳溶液区分直馏汽油和裂化汽油 | |
| B. | 蛋白质溶液中加入浓的硫酸铵溶液会有蛋白质析出 | |
| C. | 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应 | |
| D. | 相对分子质量相近的醇和烷烃,烷烃的沸点远远高于醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用湿润的pH试纸测定溶液的pH,测定结果偏小,该溶液一定呈酸性 | |
| B. | 用pH试纸分别测定氯水和盐酸的pH值,比较两溶液的酸性强弱 | |
| C. | 取同体积不同浓度的醋酸和盐酸加水稀释相同倍数,测定稀释前后pH值的变化,以此区别这两种酸 | |
| D. | 测定硫酸型酸雨的pH值时,取样后应立即测定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 进行萃取操作时,应选择有机萃取剂,且萃取剂的密度要比水大 | |
| B. | 进行蒸馏操作时,应使温度计的水银球靠近蒸馏烧瓶的瓶口处 | |
| C. | 进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 进行蒸发操作时,应将蒸发皿中溶液蒸干后,再停止加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com