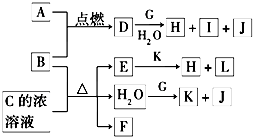
如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,D的溶液呈棕黄色;组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.
回答下列问题:
(1)K的化学式
NaOH
NaOH
,H的化学式
Fe(OH)3
Fe(OH)3
(2)D的水溶液与G反应的离子方程式为
2Fe3++6H2O+6Na=2Fe(OH)3↓+6Na++3H2↑或2Na+2H2O═2Na++2OH-+H2↑,Fe3++3OH-=Fe(OH)3↓
2Fe3++6H2O+6Na=2Fe(OH)3↓+6Na++3H2↑或2Na+2H2O═2Na++2OH-+H2↑,Fe3++3OH-=Fe(OH)3↓
.
(3)将F通入D的水溶液中反应的离子方程式为
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
.
(4)少量B与C的浓溶液加热时反应的化学方程式为:
2Fe+6H
2SO
4(浓)
Fe
2(SO
4)
3+3SO
2↑+6H
2O
2Fe+6H
2SO
4(浓)
Fe
2(SO
4)
3+3SO
2↑+6H
2O
.

 如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,D的溶液呈棕黄色;组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.
如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,D的溶液呈棕黄色;组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.

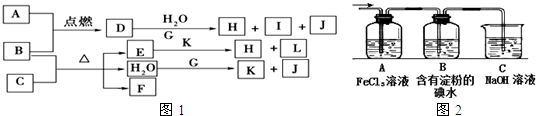
 回答下列问题:
回答下列问题: 如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,D的溶液呈棕黄色;组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.
如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,D的溶液呈棕黄色;组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色. 如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,D的溶液呈棕黄色;组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.
如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,D的溶液呈棕黄色;组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.