设NA表示阿伏伽德罗常数,下列说法正确的是( )
A.在25℃、101kPa下,11.2L氧气所含的原子数为NA
B.0.5molNa与足量水发生反应转移的电子数为NA
C.20g重水(D2O)所含的电子数为10NA
D.在标准状况下,5.6L的CCl4中所含的氯原子总数为NA
【答案】
分析:A、气体摩尔体积v
m=22.4L/mol的使用条件是标准状况(0℃、101kPa);
B、Na与水发生反应生成钠离子,一个钠原子失去一个电子生成钠离子,所以转移的电子数与钠原子数相等;
C、求出重水的物质的量,由于一个重水分子中含有10个电子,再根据N(电子数)=10n(D
2O)N
A计算;
D、气体摩尔体积v
m=22.4L/mol的使用范围是单一气体或能共存的混合气体(在标准状况下),
解答:解:A、不是标准状况,不能使用气体摩尔体积v
m=22.4L/mol,故A错误.
B、Na与水发生反应生成钠离子,一个钠原子失去一个电子生成钠离子,所以转移的电子数与钠原子数相等,为0.5N
A,故B错误.
C、n(D
2O)=
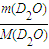
=
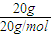
=1mol,20g重水(D
2O)所含的电子数为N(电子数)=)=10n(D
2O)N
A=10N
A,故C错误.
D、标况下,CCl
4是液体,气体摩尔体积v
m=22.4L/mol不适用于该物质,所以5.6L的CCl
4中所含的氯原子总数不是N
A,故D错误.
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,难度不大,注意气体摩尔体积的使用范围和条件及重水的摩尔质量.

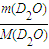 =
=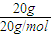 =1mol,20g重水(D2O)所含的电子数为N(电子数)=)=10n(D2O)NA=10NA,故C错误.
=1mol,20g重水(D2O)所含的电子数为N(电子数)=)=10n(D2O)NA=10NA,故C错误.

 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案