
 ČēĶ¼ŹĒæÉÄę·“Ó¦X2+3Y2?2Z2 ŌŚ·“Ó¦¹ż³ĢÖŠµÄ·“Ó¦ĖŁĀŹ£ØV£©ÓėŹ±¼ä£Øt£©µÄ¹ŲĻµĒśĻߣ¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼ŹĒæÉÄę·“Ó¦X2+3Y2?2Z2 ŌŚ·“Ó¦¹ż³ĢÖŠµÄ·“Ó¦ĖŁĀŹ£ØV£©ÓėŹ±¼ä£Øt£©µÄ¹ŲĻµĒśĻߣ¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | t2Ź±£¬·“Ó¦µ½“ļĻŽ¶Č | B£® | t2-t3£¬·“Ó¦ČŌŌŚ½ųŠŠ | ||
| C£® | t1Ź±£¬Ö»ÓŠÕż·½Ļņ·“Ó¦ | D£® | t2-t3£¬ø÷ĪļÖŹµÄÅØ¶Č²»ŌŁ·¢Éś±ä»Æ |
·ÖĪö A”¢t2Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąĶ¬£¬·“Ó¦“ļĘ½ŗāדĢ¬£¬“ĖĢõ¼žĻĀ·“Ó¦µ½“ļĻŽ¶Č£»
B£®t2-t3Ź±ÕżÄę·“Ó¦ĖŁĀŹĻąĶ¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬ŹĒ¶ÆĢ¬Ę½ŗā£¬vÕżØTvÄę£¾0£»
C”¢t1Ź±£¬¼ČÓŠÕż·½Ļņ·“Ó¦£¬ÓÖÓŠÄę·“Ó¦£»
D”¢t2-t3£¬“ļĘ½ŗāדĢ¬£¬Ę½ŗāµÄ±źÖ¾ŹĒø÷ĪļÖŹµÄÅØ¶Č²»ŌŁ·¢Éś±ä»Æ£®
½ā“š ½ā£ŗA”¢Ķ¼Ļó·ÖĪöæÉÖŖt2Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąĶ¬£¬·“Ó¦“ļĘ½ŗāדĢ¬£¬“ĖĢõ¼žĻĀ·“Ó¦µ½“ļ×ī“óĻŽ¶Č£¬¹ŹAÕżČ·£»
B”¢t2-t3Ź±ÕżÄę·“Ó¦ĖŁĀŹĻąĶ¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬vÕżØTvÄę£¾0£¬ŹĒ¶ÆĢ¬Ę½ŗā£¬·“Ó¦ČŌŌŚ½ųŠŠ£¬¹ŹBÕżČ·£»
C”¢t1Ź±£¬¼ČÓŠÕż·½Ļņ·“Ó¦£¬ÓÖÓŠÄę·“Ó¦£¬Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬·“Ó¦ÕżĻņ½ųŠŠ£¬·“Ó¦Ī““ļµ½Ę½ŗāדĢ¬£¬¹ŹC“ķĪó£»
D”¢t2-t3£¬ÕżÄę·“Ó¦ĖŁĀŹĻąĶ¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬“ļĘ½ŗāדĢ¬Ź±ø÷ĪļÖŹµÄÅØ¶Č²»ŌŁ·¢Éś±ä»Æ£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖæÉÄę·“Ó¦µÄ¶ØŅå¼°»ÆŃ§Ę½ŗāדĢ¬µÄÅŠ¶Ļ£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņā»ÆŃ§Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬µ«²»ĪŖ0ŹĒ¶ÆĢ¬Ę½ŗā£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | I- | B£® | HCO${\;}_{3}^{-}$ | C£® | Cl- | D£® | NO${\;}_{3}^{-}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
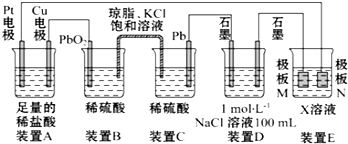
| A£® | »ŌŹÆ”¢Š±³¤ŹÆ¼°éĻéŹÆ¾łŹōÓŚ¹čĖįŃĪæó | |
| B£® | éĻéŹÆÖŠĢśĪŖ+2¼Ū | |
| C£® | ŌĀĒņ±ķ²ćɳĶĮÖŠÓŠÓĪĄėĢ¬ĢśŹĒŅņĪŖŌĀĒņµÄ±ķĆę¼øŗõƻӊŃõĘų | |
| D£® | Š±³¤ŹÆµÄŃõ»ÆĪļŠĪŹ½æɱķŹ¾ĪŖ£ŗK2O•Al2O3•3SiO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com