
【题目】利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法正确的是
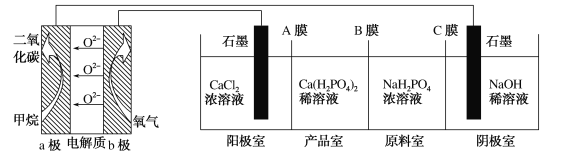
A.a极反应:CH4+8e-+4O2-=CO2+2H2O
B.A膜和C膜均为阴离子交换膜
C.可用铁电极替换阴极的石墨电极
D.a极上通入2.24 L甲烷,阳极室Ca2+减少0.4 mol
 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】制取水煤气反应C(s)+H2O(g)CO(g)+H2(g),化学平衡常数表示为K=![]() ,有关化学平衡常数说法正确的是( )
,有关化学平衡常数说法正确的是( )
A.由表达式可知c(CO)与c(CO)增大时,K值增大
B.其他条件不变时,温度升高,K值增大
C.化学平衡向右移动,K值增大
D.K值变化,化学平衡一定发生了移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为![]() 的
的![]() 溶液和
溶液和![]() 溶液按体积分别为Va和Vb混合,保持
溶液按体积分别为Va和Vb混合,保持![]() ,且生成的
,且生成的![]() 可溶于水。已知
可溶于水。已知![]() 与混合液pH关系如图。下列说法错误的是( )
与混合液pH关系如图。下列说法错误的是( )
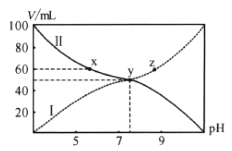
A.曲线Ⅰ表示![]() 溶液体积B.
溶液体积B.![]() 点存在
点存在![]()
C.电离平衡常数![]() D.向
D.向![]() 点溶液加入
点溶液加入![]() ,水的电离程度减小
,水的电离程度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HA的酸性弱于HB的酸性。25℃时,用NaOH固体分别改变物质的量浓度均为0.1molL-1的HA溶液和HB溶液的pH(溶液的体积变化忽略不计),溶液中A-、B-的物质的量浓度的负对数与溶液的pH的变化情况如图所示。下列说法正确的是( )
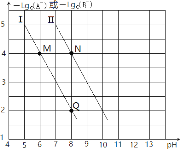
A.曲线Ⅰ表示溶液的pH与-lgc(A-)的变化关系
B.![]() =1000
=1000
C.溶液中水的电离程度:M>N
D.N点对应的溶液中c(Na+)<Q点对应的溶液中c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥美拉唑主要用于十二指肠溃疡和胃溃的治疗,静脉注射可用于消化性溃疡急性出血的治疗,反应中间体F和奥美拉唑的合成路线如图:
I>中间体F的合成:
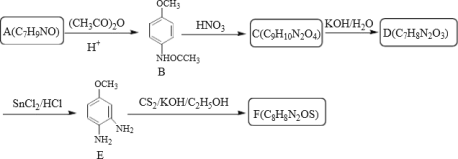
II.奧美拉唑的合成:
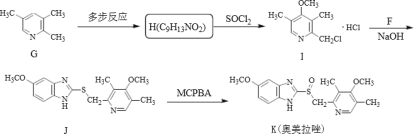
已知:R-OH![]() R-Cl
R-Cl
R1-SH+R2-X![]() R1-S-R2
R1-S-R2
结合上述合成路线,请回答:
(1)下列说法正确的是_____。
A.奥美拉唑的分子式为C18H19N3O3S
B.J生成K的反应类型为加成反应
C.化合物C可以发生的反应类型有取代、还原、加成
D.设计A转化为B的目的是保护其中的官能团
(2)化合物F的结构简式为_____;
(3)请写出A→B的反应方程式_____;
(4)试写出同时满足下列条件的化合物H的同分异构体:_____。
①分子中含苯环,遇FeC13显紫色
②分子中含有4种不同化学环境的氢原子。
(5)利用已有知识和题中涉及的反应,设计从乙烯合成![]() 的路线_____。(用流程图表示,无机试剂任选)
的路线_____。(用流程图表示,无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴、铜及其化合物在工业上有重要用途,回答下列问题:
(1) 请补充完基态Co的简化电子排布式:[Ar]______, Co2+有________个未成对电子。
(2)Na3[Co(NO2)6]常用作检验K+的试剂, 配位体![]() 的中心原子的杂化形式为______, 空间构型为______。大π键可用符号
的中心原子的杂化形式为______, 空间构型为______。大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为![]() ,则
,则![]() 中大π键应表示为________。
中大π键应表示为________。
(3)配合物[Cu(En)2]SO4的名称是硫酸二乙二胺合铜(Ⅱ), 是铜的一种重要化合物。其中 En 是乙二胺(H2NCH2CH2NH2)的简写。
①该配合物[Cu(En)2]SO4中N、 O、 Cu的第一电离能由小到大的顺序是__________。
②乙二胺和三甲胺[N(CH3)3]均属于胺, 且相对分子质量相近, 但乙二胺比三甲胺的沸点高得多, 原因是___________
(4) 金属Cu晶体中的原子堆积方式如图所示, 其配位数为________,铜原子的半径为a nm, 阿伏加德罗常数的值为NA, Cu的密度为________ g/cm3(列出计算式即可)。
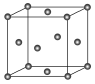
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值,下列有关叙述正确的是()
A.将78gNa2O2与过量CO2反应转移的电子数为2NA
B.1molN2与4molH2反应生成的NH3分子数为2NA
C.标准状况下,2.24LSO3中所含原子数为0.4NA
D.标准状况下,18gD2O中所含电子数为9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO是重要化学物质。回答下列问题:
(1)工业生产硝酸时,首先氨氧化反应制备NO,写出该反应的化学方程式:_____________。
(2)工厂排放尾气中NO可用催化剂[La0.8A0.2BCoO3+x(A.B均为过渡元素)]脱除。研究表明,一定温度下,NO的脱除率与还原剂(如H2)、催化剂以及催化剂表面氧缺位(※)的密集程度有关。催化机理如下:
第一阶段:B4+(不稳定)+H2→低价态的金属离子(还原前后催化剂中金属原子的个数不变)
第二阶段:NO(g)+※→NO(吸附态) H1、K1
2NO(吸附态)→2N(吸附态)+O2(g) △H2、K2
2N(吸附态)→N2(g)+2※ △H3、K3
2NO(吸附态)→N2(g) +2O(吸附态) H4、K4
2O(吸附态)→O2(g)+2※ △H5、K5
①第一阶段用H2还原B4+得到低价态的金属离子越多,第二阶段反应的速率越快,其原因是__________________________________。
②根据第二阶段可知,能量大小:NO(g)__________(填“>”“=”或“<”)NO(吸附态)。
③该温度下,NO脱除反应2NO(g)![]() N2(g)+ O2(g)的平衡常数K=_____(用K1、K4、K5的表达式表示)。
N2(g)+ O2(g)的平衡常数K=_____(用K1、K4、K5的表达式表示)。
(3)物质的生成热是指最稳定的单质合成1mol该物质所放出的热量(H);单质的生成热均为0。已知NO(g)、CO(g)、CO2(g)的生成热分别为90.4kJ·mol-1、l10kJ·mol-1、393 kJ·mol-1。则一定条件下,NO(g)与CO(g)反应2NO(g) + 2CO(g)![]() N2(g)+2CO2(g)的△H=_____。
N2(g)+2CO2(g)的△H=_____。
(4)在2 L恒容密闭容器中充入4 mol CO和4 mol NO,发生反应2NO(g) +2CO(g)![]() N2(g)+ 2CO2(g),平衡时,NO的体积分数与温度(℃)、压强(Pa)的关系如图所示。
N2(g)+ 2CO2(g),平衡时,NO的体积分数与温度(℃)、压强(Pa)的关系如图所示。
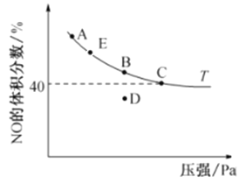
①C点NO的平衡转化率为______;若C点在10 min达到平衡,则10 min内CO的平均反应速率为________。
②若起始容器内压强为力P,则C点时该反应的平衡常数Kp=____ (用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
③若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是________________(从图中A、B、C、E点选填)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的化工原料,可由乙烷为原料制取,回答下列问题。
(1)传统的热裂解法和现代的氧化裂解法的热化学方程式如下:
①C2H6(g)=C2H4(g)+H2(g) ΔH1=+136kJ·mol-1
②C2H6(g)+![]() O2(g)=C2H4(g)+H2O(g) ΔH2=-110kJ·mol-1
O2(g)=C2H4(g)+H2O(g) ΔH2=-110kJ·mol-1
已知反应相关的部分化学键键能数据如下:
化学键 | H-H(g) | H-O(g) | O=O |
键能(kJ·mol-1) | 436 | x | 496 |
由此计算x=___,通过比较ΔH1和ΔH2,说明和热裂解法相比,氧化裂解法的优点是___(任写一点)。
(2)乙烷的氧化裂解反应产物中除了C2H4外,还存在CH4、CO、CO2等副产物(副反应均为放热反应),图甲为温度对乙烷氧化裂解反应性能的影响。乙烷的转化率随温度的升高而升高的原因是___,反应的最佳温度为___(填序号)。
A.700℃ B.750℃ C.850℃ D.900℃

[乙烯选择性=![]() ;乙烯收率=乙烷转化率×乙烯选择性]
;乙烯收率=乙烷转化率×乙烯选择性]
(3)烃类氧化反应中,氧气含量低会导致反应产生积炭堵塞反应管。图乙为![]() 的值对乙烷氧化裂解反应性能的影响。判断乙烷氧化裂解过程中
的值对乙烷氧化裂解反应性能的影响。判断乙烷氧化裂解过程中![]() 的最佳值是___,判断的理由是___。
的最佳值是___,判断的理由是___。
(4)工业上,保持体系总压恒定为100kPa的条件下进行该反应,通常在乙烷和氧气的混合气体中掺混惰性气体(惰性气体的体积分数为70%),掺混惰性气体的目的是___。反应达平衡时,各组分的体积分数如下表:
组分 | C2H6 | O2 | C2H4 | H2O | 其他物质 |
体积分数/% | 2.4 | 1.0 | 12 | 15 | 69.6 |
计算该温度下的平衡常数:Kp=___(用平衡分压代替平衡浓度,平衡分压=总压×体积分数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com