
| A. | ①<②<③ | B. | ①<③<② | C. | ③<②<① | D. | ③<①<② |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
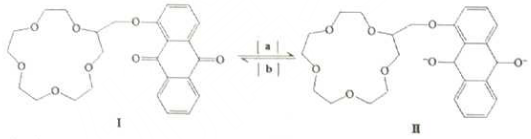
| A. | 物质Ⅰ的分子式是C25H28O8 | B. | 反应[a]是氧化反应 | ||
| C. | 1molⅠ可与8molH2发生加成反应 | D. | 物质Ⅰ的所有原子不可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水鉴别苯和正己烷 | |
| B. | 煤气的主要成分是丁烷 | |
| C. | 石油是混合物,其分馏产品汽油为纯净物 | |
| D. | 石油催化裂化的主要目的是提高汽油等轻质油的产量与质量,石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20g D2O中含的质子数为10NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 46g NO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 常温下,22.4L CO2气体的分子总数小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、烧碱、醋酸钠、AlO2•2SiO2•2H2O分别属于酸、碱、盐和氧化物 | |
| B. | 蔗糖、硝酸钾和硫酸钡分别属于非电解质、强电解质和弱电解质 | |
| C. | CuSO4•5H2O、冰醋酸、冰水混合物属于纯净物;水玻璃、氢氧化铁胶体属于混合物 | |
| D. | SO2、SiO2、CO属于酸性氧化物;CuO、Fe2O3、Na2O2属于碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝具有良好导热性,可用铝罐贮运浓硝酸 | |
| B. | 水玻璃能与酸反应,可用作生产黏合剂和防火剂 | |
| C. | NaNO2具有碱性,可用于使铁零件表面生成Fe3O4 | |
| D. | FeCl3溶液能与Cu反应,可用作铜制线路板的蚀刻剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度能使化学反应速率增大,主要原因是增加了活化分子的百分数,从而使有效碰撞频率提高 | |
| B. | 增大气体反应的压强,单位体积中活化分子数增多,气体反应速率加快 | |
| C. | 增大反应物的浓度,活化分子百分数增加,反应速率加快 | |
| D. | 催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com