
| A. | c(C2O42-)+c(HC2O4-)+c(OH-)=c(K+)+c(H+) | |
| B. | c(C2O42-)+c(HC2O4-)+c(H2C2O4)=0.2mol/L | |
| C. | c(C2O42-)<c(HC2O4-)<c(H2C2O4) | |
| D. | c(C2O42-)+c(HC2O4-)+c(H2C2O4)<c(K+) |
分析 向100mL0.2mol/L的草酸溶液中加入1.68 g KOH固体,n(H2C2O4)=0.02mol,n(KOH)=$\frac{1.68g}{56g/mol}$=0.03mol,则二者反应生成0.01molK2C2O4、0.01molKHC2O4,由KHC2O4溶液呈酸性,则混合溶液显酸性,电离大于水解,结合物料守恒及电荷守恒解答.
解答 解:向100mL0.2mol/L的草酸溶液中加入1.68 g KOH固体,n(H2C2O4)=0.02mol,n(KOH)=$\frac{1.68g}{56g/mol}$=0.03mol,则二者反应生成0.01molK2C2O4、0.01molKHC2O4,由KHC2O4溶液呈酸性,则混合溶液显酸性,电离大于水解,
A.由电荷守恒可知,存在2c(C2O42-)+c(HC2O4-)+c(OH-)=c(K+)+c(H+),故A错误;
B.由草酸根中C原子守恒,可知物料守恒式为c(C2O42-)+c(HC2O4-)+c(H2C2O4)=0.2mol/L,故B正确;
C.混合溶液显酸性,电离大于水解,则c(H2C2O4)<c(HC2O4-)<c(C2O42-),故C错误;
D.溶液中存在物料守恒3[c(C2O42-)+c(HC2O4-)+c(H2C2O4)]=2c(K+),则c(C2O42-)+c(HC2O4-)+c(H2C2O4)<c(K+),故D正确;
故选AC.
点评 本题考查离子浓度大小的比较及酸碱混合计算,把握混合后溶液中溶质及量的关系为解答的关键,注意电荷守恒及物料守恒的应用,注意D中的等量代换,题目难度不大.


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:解答题
| 实验 编号 | T/K | 催化剂的 用量/g | KMnO4酸性溶液 的浓度/mol?L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究催化剂对该反应速率的影响 |
| ② | ||||
| ③ | ||||
| ④ |
| KMnO4酸性溶液的浓度/mol.L-1 | 溶液褪色所需时间t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g H2O含有3NA个原子 | |
| B. | 1 mol甲苯含有6NA个C-H键 | |
| C. | 标准状况下,22.4 L氯水含有NA个Cl2分子 | |
| D. | 2.8 g乙烯和丁烯的混合气体中所含原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2的摩尔质量是2 g | B. | 1 mol H2O的质量是18 g/mol | ||
| C. | 氧气的摩尔质量是32 g/mol | D. | 2 g H2含1 mol H |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
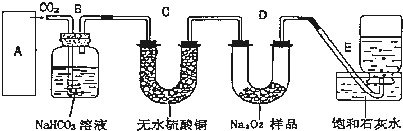
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水电解生成氢气和氧气,说明水中含有氢分子和氧分子 | |
| B. | 用肥皂水不可以区分硬水和软水 | |
| C. | 将黄河水经沉降、过滤、吸附,灭菌等净化操作后,可供人们生活用水 | |
| D. | 水体有一定的自净功能,部分工业污水可直接排放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com