
分析 分子通式均为CnH2n+2O的A、B、C三种有机物,均能与钠反应产生H2,应含有羟基,为饱和一元醇,相同条件下A的蒸气密度与O2相同,应为CH3OH;相同质量的A和B在相同条件下的蒸气体积比为11:4,则相对分子质量之比为4:11,B的相对分子质量为88,分子式应为C5H12O;B与C互为同分异构体.并知B可催化氧化成醛而不能脱水成烯,说明含有-CH2OH,且邻位碳原子不含H原子;C可以脱水得烯,但不能催化氧化得醛,说明邻位碳原子含有H原子,但不含-CH2OH结构,以此解答该题.
解答 解:分子通式均为CnH2n+2O的A、B、C三种有机物,均能与钠反应产生H2,应含有羟基,为饱和一元醇,相同条件下A的蒸气密度与O2相同,应为CH3OH;相同质量的A和B在相同条件下的蒸气体积比为11:4,则相对分子质量之比为4:11,B的相对分子质量为88,分子式应为C5H12O;B与C互为同分异构体.并知B可催化氧化成醛而不能脱水成烯,说明含有-CH2OH,且邻位碳原子不含H原子,应为(CH3)3CCH2OH;C可以脱水得烯,但不能催化氧化得醛,说明邻位碳原子含有H原子,但不含-CH2OH结构,应为(CH3)2COHC2H5,
故答案为:CH3OH;(CH3)3CCH2OH;(CH3)2COHC2H5.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析、计算能力的考查,注意把握有机物的结构和性质的关系,把握同分异构体的判断,难度中等.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
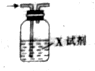 已知CO2通入澄清石灰水中,溶液先变浑浊,后又变澄清.用如图装置除去CO2气体中的HCl,X试剂最合适的是( )
已知CO2通入澄清石灰水中,溶液先变浑浊,后又变澄清.用如图装置除去CO2气体中的HCl,X试剂最合适的是( )| A. | NaOH溶液 | B. | 浓硫酸 | C. | Na2CO3溶液 | D. | NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
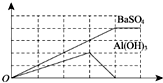 已知向溶液Q中滴加溶液P可生成两种沉淀,所得沉淀量与所加入的P溶液的体积关系如图所示,则Q、P分别为( )
已知向溶液Q中滴加溶液P可生成两种沉淀,所得沉淀量与所加入的P溶液的体积关系如图所示,则Q、P分别为( )| A. | Q为NH4Al(SO4)2,P为Ba(OH)2 | B. | Q为Ba(OH)2,P为明矾 | ||
| C. | Q为明矾,P为Ba(OH)2 | D. | Q为Ba(AlO2)2,P为硫酸铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验方案(只要求填写选用试剂) | (1) | (2) |
| AlCl3溶液、MgCl2溶液、NaOH溶液 | 氯水、NaBr溶液 | |
| 实验现象 | 针对方程式①②或③试管中先生成白色沉淀,后白色沉淀消失. 针对方程式④:试管中有白色沉淀. | 溶液由浅黄绿色变成橙黄色 |
| 有关反应的离子方程式 | ①Al3++3OH-═Al(OH)3↓ ②Al(OH)3+OH-═AlO-2+H2O 或③Al3++4OH-═AlO-2+2H2O ④Mg2++2OH-═Mg(OH)2↓ | 2Br-+Cl2═Br2+2Cl- |
| 结论 | 金属性:Mg>Al | 非金属性:Cl>Br |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
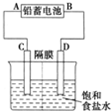 如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极).
如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醛 | B. | 甲醛 | C. | 丙醛 | D. | 丁醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a可能等于b | B. | a一定大于b | C. | a可能大于b | D. | a一定等于b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com