
| A. | NO3-、K+、Cl-、I- | B. | NH4+、Na+、SO42-、Ba2+ | ||
| C. | Na+、SO42-、HCO3-、K+ | D. | Mg2+、Cl-、SO42-、Na+ |
分析 能够与氢气反应生成氢气,则该溶液为酸性溶液,溶液中存在大量的氢离子,
A.硝酸根离子在酸性条件下具有强氧化性,能够氧化碘离子;
B.钡离子和硫酸根离子反应生成硫酸钡沉淀;
C.碳酸氢根离子与氢离子反应生成二氧化碳气体和水;
D.四种离子之间不发生反应,都不与氢离子反应.
解答 解:该溶液为酸性溶液,溶液中存在大量氢离子,
A.NO3-、I-之间在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.SO42-、Ba2+之间反应生成难溶物硫酸钡,在溶液中不能大量共存,故B错误;
C.HCO3-与氢离子反应生成二氧化碳气体,在溶液中不能大量共存,故C错误;
D.Mg2+、Cl-、SO42-、Na+之间不发生反应,都不与氢离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识的能力.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:解答题
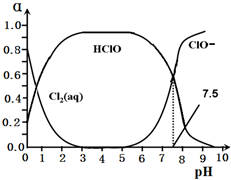 元素周期表中ⅦA族元素的单质及其化合物的用途广泛.
元素周期表中ⅦA族元素的单质及其化合物的用途广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物 的名称为2,6-二甲基-5-乙基庚烷 的名称为2,6-二甲基-5-乙基庚烷 | |
| B. | 乙烯和聚乙烯二者都能使溴的四氯化碳溶液褪色 | |
| C. | 化合物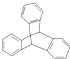 是苯的同系物 是苯的同系物 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA | |
| B. | 0.5molC3H8分子中所含C-H共价键数为2NA | |
| C. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| D. | 1mol碳正离子CH3+所含的电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
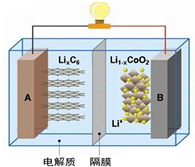 随着各地“限牌”政策的推出,电动汽车成为汽车届的“新宠”. 特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图,A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许 Li+通过,电池反应式LixC6+Li1-xCoO2$?_{充电}^{放电}$C6+LiCoO2.下列说法不正确的是( )
随着各地“限牌”政策的推出,电动汽车成为汽车届的“新宠”. 特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图,A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许 Li+通过,电池反应式LixC6+Li1-xCoO2$?_{充电}^{放电}$C6+LiCoO2.下列说法不正确的是( )| A. | 充电时Li+从右边流向左边 | |
| B. | 放电时,正极锂的化合价未发生改变 | |
| C. | 充电时B作阳极,该电极放电时的电极反应式为:Li1-x CoO2+xLi++xe-=LiCoO2 | |
| D. | 废旧钴酸锂(LiCoO2)电池进行“放电处理”让Li+进入石墨中而有利于回收 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的金属性比Y的金属性强 | |
| B. | 常温下,X和Y都不能从水中置换出氢 | |
| C. | Y元素的氢氧化物碱性比X 元素的氢氧化物碱性强 | |
| D. | X元素的最高化合价比Y 元素的最高化合价低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑥ | B. | ①③⑥ | C. | ②④⑥ | D. | ①②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com