
(12分)某强酸性溶液X中仅含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下:

根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的阳、阴离子分别是_____________。
(2)用离子方程表达下列反应:
①中生成气体A:___________ __。
②中生成溶液H:____________ _。
(3)若②中所用氢氧化钠浓度为2mol/L,当加入l0 ml时开始产生沉淀,55 ml时沉淀的量达到最大值0.03 mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60ml时沉淀的量降为0.025 mol且保持不变,则原溶液中c(Fe2+)为___________mol/L、c(Fe3+)为___________mol/L、c(Cl-)为___________mol/L。(若有些离子不存在,请填0 mol/L)
(每空2分 共14分)(1) Fe3+ 、Cl-
(2)3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
Al3+ +4OH-=AlO2-+2H2O
(3)0.15 0.1 0
【解析】
试题分析:强酸性溶液中一定不存在CO32-、SO32-,则与过量的硝酸钡溶液反应,生成9.32g沉淀,则该沉淀是硫酸钡沉淀,物质的量是9.32g/233g/mol=0.04mol,说明溶液中存在0.04mol SO42-,则一定不存在Ba2+;与过量硝酸钡反应生成的气体A可连续被氧化,说明A是NO,D是二氧化氮,则溶液中存在与硝酸发生氧化还原反应的离子,为Fe2+,所以溶液中一定不存在NO3-;溶液B中含有铁离子和过量的硝酸钡,加入氢氧化钠溶液仍产生气体,说明原溶液中存在NH4+,氨气的物质的量也是铵根离子的物质的量是0.112L/22.4L/mol=0.005mol;则沉淀G中一定含有氢氧化铁;通入过量的二氧化碳,仍能产生沉淀,因为铁离子上步中被完全沉淀,所以此时产生的沉淀只能是氢氧化铝,说明溶液中存在铝离子;而Fe3+ 、Cl-不能确定。
(1)根据以上分析,不能确定溶液X中是否含有的阳、阴离子分别是Fe3+ 、Cl-;
(2)①硝酸与亚铁离子发生氧化还原反应生成铁离子、NO和水,离子方程式是3Fe2++4H++NO3-=3Fe3++NO↑+2H2O;
②中生成溶液H,即为铝离子和过量的氢氧化钠反应生成偏铝酸钠和水,离子方程式是Al3+ +4OH-=AlO2-+2H2O;
(3)根据生成NO的体积可计算亚铁离子的浓度,NO的物质的量是0.112L/22.4L/mol=0.005mol,则亚铁离子的物质的量是0.005mol×3=0.015mol,c(Fe2+)=0.015mol/0.1L=0.15mol/L;加入氢氧化钠溶液60mL时沉淀量降到0.025mol,说明此时为氢氧化铁沉淀,亚铁离子的物质的量是0.015mol,所以说明原溶液中存在铁离子,其物质的量是0.025mol-0.015mol=0.01mol,则c(Fe3+)=0.01mol/0.1L=0.1mol/L;加入55mL氢氧化钠溶液时沉淀达到最大值0.03mol,加入60mL氢氧化钠溶液时,沉淀降为0.025mol,说明氢氧化铝的物质的量是0.03mol-0.025mol=0.005mol,则溶液中SO42-:0.04mol,NH4+:0.005mol,Fe2+:0.015mol,Fe3+:0.01mol,Al3+:0.005mol,此时2n(SO42-)=n(NH4+)+2n(Fe2+)+3n(Fe3+)+3n(Al3+),所以c(Cl-)=0mol/L。
考点:考查离子的检验与计算


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源:2014-2015学年广东省清远市高三上学期期末理综化学试卷(解析版) 题型:选择题
(16分)某小组进行铝热反应实验,装置如图所示。
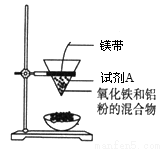
(1)铝热反应原理 (写化学方程式),试剂A为 (写化学式)。
(2)对坩埚内的黑色固体物质的组成,小组进行了如下探究
假设I:该黑色物质为铁
假设Ⅱ:该黑色物质为铁与氧化铁的混合物
【设计方案并实验】
实 验 步 骤 | 现 象 | 结 论 |
①取少量黑色固体于试管中加稀盐酸 | 固体全部溶解,有气泡产生 | 假设I成立,假设Ⅱ不成立 |
②滴入几滴0.01mol/LKSCN溶液 | 溶液不变色 |
【交流评价】
你认为上述结论是否合理? ,理由是 。
(3)取上述实验所得溶液,滴入适量氯水溶液变红色。
①此时涉及的氧化还原反应的离子反应方程式为 。
②利用反应体系中存在的平衡:Fe3++3SCN— Fe(SCN)3,小组再将滴入适量氯水的溶液平均分成两份,分别置于两支试管中并编号l、2,进行如下表所示的探究。该实验中,小组主要探究的问题是 ;应重点观察的现象是 ;预计得出的结论是 。
Fe(SCN)3,小组再将滴入适量氯水的溶液平均分成两份,分别置于两支试管中并编号l、2,进行如下表所示的探究。该实验中,小组主要探究的问题是 ;应重点观察的现象是 ;预计得出的结论是 。
实验编号 | 实验步骤 |
1 | ①滴加饱和FeCl3溶液4滴,充分振荡 |
②滴加几滴NaOH溶液 | |
2 | ①滴加4滴1mol/LKSCN溶液 |
②滴加几滴NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省茂名市高三一模考试理综化学试卷(解析版) 题型:选择题
常温下,各1L的 0.1 mol·L-1的HX溶液与0.1 mol·L-1某一元碱ROH溶液加水稀释,两溶液pH与加水体积变化曲线如图,下列说法正确的是
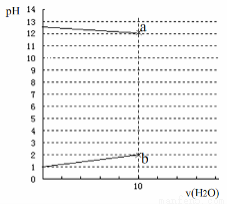
A.HX为一种弱酸,ROH为弱碱
B.a、b两点由水电离出c(H+)均为10-12mol·L-1
C.两溶液等体积混合: c(X-) = c(R+)+ c(ROH)
D.两溶液等体积混合:c(R+)>c(X-)>c(OH-) >c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:填空题
【选修5—有机化学基础】(14分)
有机物AM有如图所示转化关系,A与F分子中所含碳原子数相同,且均能与 NaHCO3溶液反应;F的分子式为C9H10O2,且不能使溴的CCl4溶液褪色;D能发生银镜反应;M.与NaOH溶液反应后的产物,其一氯代物只有一种。

请回答:
(1)B、F的结构简式分别为____________、____________
(2)反应①⑦中,属于消去反应的是________(填反应序号)。
(3)D发生银镜反应的化学方程式为_______________________;反应⑦的化学方程式为________________________
(4)A的相对分子质量在180260之间,从以上转化中不能确认A中的某一官能团,确 定该官能团的实验步骤和现象为________________________________________
(5)符合下列条件的F的同分异构体共有________种。
a.能发生银镜反应
b.能与FeCl3溶液发生显色反应
c.核磁共振氢谱上有四个峰,其峰面积之比为1:1:2:6
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:选择题
下列图中的实验方案,能达到实验目的的是:
A | B | C | D | |
实验 方案 |
|
|
|
|
实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 制备Fe(OH)2并能较长时间观察其颜色 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:选择题
某苯的衍生物,含有两个互为对位的取代基,其分子式为C8H10O,其中不跟NaOH溶液反应的衍生物种类有:
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省福州市高三第六次月考理综化学试卷(解析版) 题型:选择题
一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应2SO2(g)+O2(g) 2SO3(g) H=-196kJ·moL1,一段时间后达平衡,反应过程中测定的部分数据见下表:
2SO3(g) H=-196kJ·moL1,一段时间后达平衡,反应过程中测定的部分数据见下表:
反应时间/min | n(SO2)/mol | n(O2)/mol |
0 | 2 | 1 |
5 | 1.2 | |
10 | 0.4 | |
15 | 0.8 |
下列说法不正确的是
A.反应在前5min的平均速率为v (SO2)=0.08mol·L1 ·min1
B.保持温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,v (正)> v (逆)
C.该温度,反应的平衡常数为11.25L·mol-1
D.相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com