
②Fe3O4+![]() Cl2+6HCl
Cl2+6HCl![]() 3FeCl3+3H2O+
3FeCl3+3H2O+![]() O2;③3FeCl3
O2;③3FeCl3![]() 3FeCl2+
3FeCl2+![]() Cl2
Cl2
这3个反应的联合与循环,用来生产能解决环境和能源问题的某种气体,该气体是( )
A.O2 B.Cl
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| 太阳光 |
| 高温 |
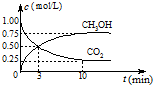
| 7 |
| 448 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上电解饱和食盐水可得到多种工业原料,其中氢气和氯气用途非常广泛.
工业上电解饱和食盐水可得到多种工业原料,其中氢气和氯气用途非常广泛.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
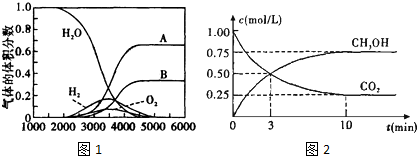
查看答案和解析>>
科目:高中化学 来源: 题型:
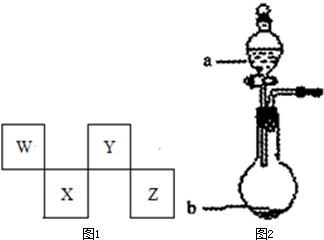
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com