
| A. | 浓NaOH溶液 | B. | 饱和食盐水 | C. | 石灰乳 | D. | 浓硫酸 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届河南省高三上第一次联考化学试卷(解析版) 题型:选择题
下列各组离子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式正确的是()
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO3-、NH4+ | NaHSO4溶液 | 3Fe2++NO3- +4H+=3 |
B | Ca2+、HCO3-、Cl- | 少量NaOH溶液 | Ca2++2HCO3- +2OH-=2H2O+CaCO3↓+CO32- |
C | K+、AlO2-、HCO3- --来源:Zxxk.Com] | 通入少量CO2 | 2Al |
D | NH4+、Al3+、SO42- | 少量Ba (OH) 2溶液 | 2NH4+ |
A.A B.B C. C D.D
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
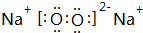
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,参加反应的HCl的物质的量为0.2mol,其中被氧化的HCl的质量3.65g.
,参加反应的HCl的物质的量为0.2mol,其中被氧化的HCl的质量3.65g.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入CH4的电极为正极 | |
| B. | 通入CH4的电极反应为:CH4+10OH-→CO32-+7H2O+8e- | |
| C. | 通入O2的电极为负极 | |
| D. | 放电时溶液中阴离子向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液物质的量浓度为10moL/L | |
| B. | 所得的溶液的体积为22.5L | |
| C. | 该溶液中溶质的质量分数因溶液的密度未知而无法求得 | |
| D. | 根据题干数据,该溶液物质的量浓度无法求得 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com