
【题目】一种以含铁废料(含Fe、FeO、Fe2O3以及不溶于酸的杂质)制备黄钠铁矾[Na2Fe6(SO4)4(OH)12]的工艺如下:

(1)“酸溶”时,硫酸应过量的原因是____和____。
(2)“氧化”的目的是____。不能用酸性KMnO4溶液检验“氧化”后的溶液中是否含有Fe2+,原因是____。(已知氧化性:酸性KMnO4>Cl2>Fe3+)
(3)如图是温度-pH与生成的含铁化合物的关系图,图中阴影部分是黄钠铁矾稳定存在的区域。
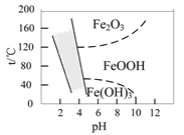
①“沉矾”反应的离子方程式为____。
②若“沉矾”反应在80℃时进行,则需控制溶液的pH范围是____。
③“氧化”后的溶液与Na2CO3溶液发生“沉矾”反应时,适宜的混合方式是____(填字母)。
a.将“氧化”后的溶液与Na2CO3溶液同时加入到反应容器中
b.将“氧化”后的溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有“氧化”后的溶液的反应容器中
【答案】使含铁废料充分溶解 抑制Fe2+、Fe3+水解 将Fe2+氧化为Fe3+ 氧化后的溶液中有Cl-,会使酸性KMnO4溶液褪色 2Na++6Fe3++4SO![]() +6CO
+6CO![]() +6H2O=Na2Fe6(SO4)4(OH)12+ 6CO2 2.5~4.1 c
+6H2O=Na2Fe6(SO4)4(OH)12+ 6CO2 2.5~4.1 c
【解析】
废催化剂加入稀硫酸,发生Co+H2SO4=CoSO4+H2↑,Fe+H2SO4=FeSO4+H2↑、FeO+H2SO4=FeSO4+H2O、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,过滤滤渣是不溶于酸的杂质,而滤液是硫酸钴、硫酸亚铁、硫酸铁与过量的硫酸的混合溶液,向滤液中加氯酸钠将亚铁离子氧化成铁离子,然后加入碳酸钠调节pH=3得到黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,过滤分离出黄钠铁矾。
(1)“酸溶”时,加入过量硫酸能使含铁废料充分溶解,同时抑制溶液中Fe2+、Fe3+水解;
(2)“氧化”的目的是将溶液中的Fe2+氧化为Fe3+;因溶液中含有Cl-,酸性KMnO4溶液同样能氧化Cl-,使溶液褪色,则无法判断 “氧化”后的溶液中是否含有Fe2+;
(3)①“沉矾”时加入碳酸钠调节pH=3得到黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,同时有CO2气体生成,则发生反应的离子方程式为2Na++6Fe3++4SO![]() +6CO
+6CO![]() +6H2O=Na2Fe6(SO4)4(OH)12+ 6CO2;
+6H2O=Na2Fe6(SO4)4(OH)12+ 6CO2;
②由图示可知,若“沉矾”反应在80℃时进行,则需控制溶液的pH范围是2.5~4.1左右;
③“氧化”后的溶液与Na2CO3溶液发生“沉矾”反应时,为准确控制溶液的pH应向“氧化”后的溶液滴加Na2CO3溶液,并控制滴加速度,防止滴加的Na2CO3溶液过量,即选项c正确,故答案为c。


科目:高中化学 来源: 题型:
【题目】在容积为 2L 的密闭容器中进行如下反应:A g + 2Bg ![]() 3Cg + nDg ,开始时 A 为 4mol,B 为 6mol,5min 末时测得 C 的物质的量为 3mol,D 的化学反应速率vD = 0.2mol L1 min1 ,请回答:
3Cg + nDg ,开始时 A 为 4mol,B 为 6mol,5min 末时测得 C 的物质的量为 3mol,D 的化学反应速率vD = 0.2mol L1 min1 ,请回答:
(1)5min 末A 的物质的量浓度为_____,
(2)前 5min 内用B 表示的化学反应速率 v(B)为_____,
(3)前 5min 内A 的转化率为_____,
(4)化学方程式中 n 的值为_____,
(5)此反应在四种不同情况下的反应速率分别为:
① v A = 5mol L1 min1 ② v B = 6mol L1 min1
③ v C = 4.5mol L1 min1 ④ v D = 8mol L1 min1
其中反应速率最快的是_____(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米铜是一种性能优异的超导材料,以辉铜矿(主要成分为Cu2S)为原料制备纳米铜粉的工艺流程如图所示:
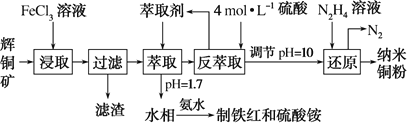
(1)用黄铜矿(主要成分为CuFeS2)、废铜渣和稀硫酸共同作用可获得较纯净的Cu2S,其原理如图所示,该反应的离子方程式为______。
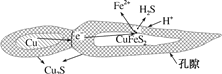
(2)从辉铜矿中浸取铜元素时,可用FeCl3溶液作浸取剂。
①反应:Cu2S+4FeCl3=2CuCl2+4FeCl2+S,每生成1mol CuCl2,反应中转移电子的物质的量为______;浸取时,在有氧环境下可维持Fe3+较高浓度,有关反应的离子方程式为______。
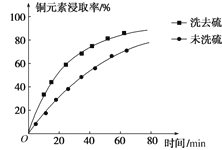
②浸取过程中加入洗涤剂溶解硫时,铜元素浸取率的变化如图所示,未洗硫时铜元素浸取率较低,其原因是______。
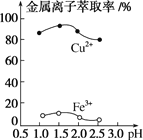
(3)“萃取”时,两种金属离子萃取率与pH的关系如图所示。当pH>1.7时,pH越大,金属离子萃取率越低,其中Fe3+萃取率降低的原因是______。
(4)用“反萃取”得到的CuSO4溶液制备纳米铜粉时,该反应中还原产物与氧化产物的质量之比为______
(5)在萃取后的“水相”中加入适量氨水,静置,再经过滤、_____、干燥、_____等操作可得到Fe2O3产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下不能实现的是( )
A.NH3![]() NO
NO![]() HNO3
HNO3
B.浓盐酸![]() Cl2
Cl2![]() 漂白粉
漂白粉
C.Al2O3![]() AlCl3(aq)
AlCl3(aq) ![]() 无水AlCl3
无水AlCl3
D.葡萄糖![]() C2H5OH
C2H5OH![]() CH3CHO
CH3CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化合物X的叙述正确的是
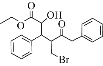
A. X分子只存在2个手性碳原子
B. X分子能发生氧化、取代、消去反应
C. X分子中所有碳原子可能在同一平面上
D. 1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如下图所示,其中A为澄清溶液,C为难溶于水的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。请回答下列问题:

(1)写出化学式:A__________C__________
(2)写出下列反应的离子方程式:
A→B:________________________________。
B→D:________________________________。
C→E:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知磷酸分子(![]() )中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸( H3 PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。下列说法正确的是
)中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸( H3 PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。下列说法正确的是
A. H3 PO2属于三元酸 B. H3 PO2的结构式为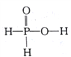
C. NaH2PO2属于酸式盐 D. NaH2PO2溶液可能呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如甲图所示[t0~t1阶段c(B)未画出]。乙图为t2时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知,t3~t4阶段使用催化剂。下列说法中不正确的是( )
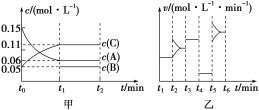
A.若t1=15 min,则用C的浓度变化表示在t0~t1时间段的平均反应速率为0.004 mol·L-1·min-1
B.t4~t5阶段改变的条件一定是减小压强
C.B的起始物质的量为0.02 mol
D.t5~t6阶段,容器内A的物质的量减少了0.03 mol,而此过程中容器与外界的热交换总量为a kJ,则该反应的热化学方程式为3A(g) B(g)+2C(g) ΔH=+100a kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中能大量共存的是( )
A.pH =1的溶液中:NH4+、SO42-、ClO-、Na+
B. 的溶液中:Na+、K+、MnO4-、HCO3-
的溶液中:Na+、K+、MnO4-、HCO3-
C.0.1molL-1的Na2SO3溶液中:H+、K+、SO42-、NO3-
D.澄清透明的溶液中:Fe3+、Na+、Cl-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com